熱線:021-66110810,66110819
手機:13564362870


熱線:021-66110810,66110819
手機:13564362870
Insights into the Production and Role of Nitric Oxide in the Antarctic Sea-ice Diatom Fragilariopsis cylindrus
南極海冰硅藻柱狀脆桿藻中一氧化氮的產(chǎn)生及作用研究
來源:Journal of Phycology,Volume56, Issue5,October 2020,Pages 1196-1207
《藻類學(xué)雜志》,第56卷,第5期,2020年10月,第1196-1207頁
摘要
摘要闡述了南極海冰硅藻柱狀脆桿藻(Fragilariopsis cylindrus)中一氧化氮(NO)的產(chǎn)生機制及其生理作用。通過微傳感器、微流體室和人工海冰槽等技術(shù),發(fā)現(xiàn)NO的產(chǎn)生依賴于亞硝酸鹽(NO??)并通過硝酸還原酶(NR)途徑。光照會抑制NO產(chǎn)生,但當(dāng)光合電子傳遞受阻(如添加抑制劑DCMU)時,光照下仍可誘導(dǎo)NO生成。外源NO會抑制藻細胞生長、破壞光合作用并改變非光化學(xué)淬滅機制。環(huán)境脅迫(鹽度、溫度變化)也會觸發(fā)NO產(chǎn)生,表明NO可能作為"脅迫信號"分子參與細胞響應(yīng)。
研究目的
1. 確定柱狀脆桿藻中NO產(chǎn)生的主要酶促途徑。
2. 探究海冰相關(guān)非生物因素(如溫度、鹽度)是否影響NO產(chǎn)生。
3. 評估外源NO對藻細胞光生理學(xué)的影響。
研究思路
1. 核心方法: 使用微流體室結(jié)合丹麥Unisense公司生產(chǎn)的Clarke型NO微電極(NO-100μm),在精確控制的微環(huán)境中實時原位監(jiān)測細胞尺度上的NO動態(tài)變化。
2. 生化途徑驗證: 在微流體室中向細胞施加不同氮源(亞硝酸鹽、硝酸鹽、L-精氨酸)及特定抑制劑(如NOS阻斷劑L-NAME、NO清除劑血紅蛋白Hb),通過電極信號變化判斷NO來源途徑。
3. 光調(diào)控研究: 在微流體室中精確控制光照條件(黑暗、低光、高光),并結(jié)合光合抑制劑DCMU處理,研究光照及光合電子傳遞對NO產(chǎn)生的影響。
4. 環(huán)境脅迫模擬: 使用溫度梯度裝置和鹽度調(diào)節(jié)培養(yǎng)液,測量不同溫度(-1.7°C至7.7°C)和鹽度(36至55)脅迫下細胞內(nèi)的NO產(chǎn)量(同樣使用Unisense電極在黑暗條件下測量)。
5. 外源NO效應(yīng): 使用NO供體SNAP處理藻細胞,利用調(diào)制葉綠素?zé)晒鈨x(Water-PAM)測量其對光合效率(Fv/Fm)、相對電子傳遞速率(rETRmax)、光化學(xué)淬滅(qP)及非光化學(xué)能量耗散組分(ΦII, ΦNPQ, ΦNO)的影響,并檢測其對細胞生長和ATP含量的影響。
6. 生態(tài)關(guān)聯(lián)驗證: 在人工倒置海冰槽中模擬海冰環(huán)境,嵌入培養(yǎng)柱進行平行實驗,比較與實驗室微流體結(jié)果的差異。
測量的數(shù)據(jù)及研究意義
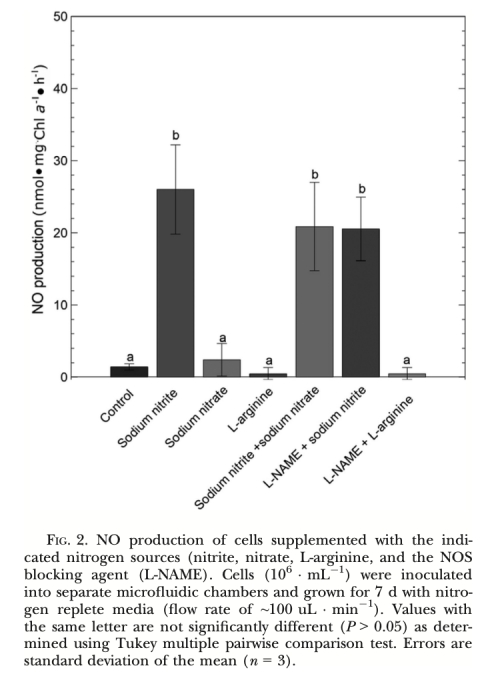
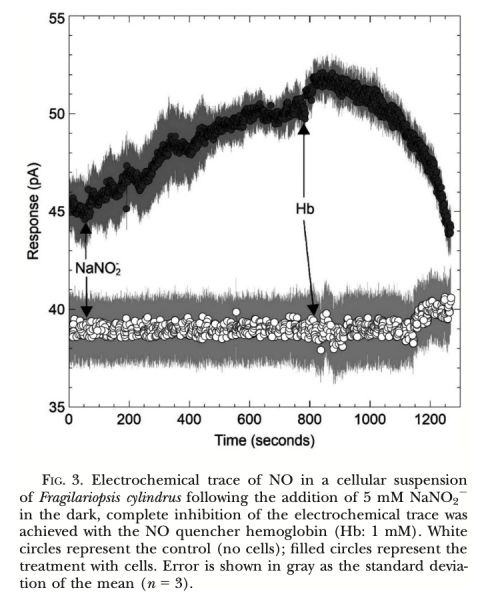
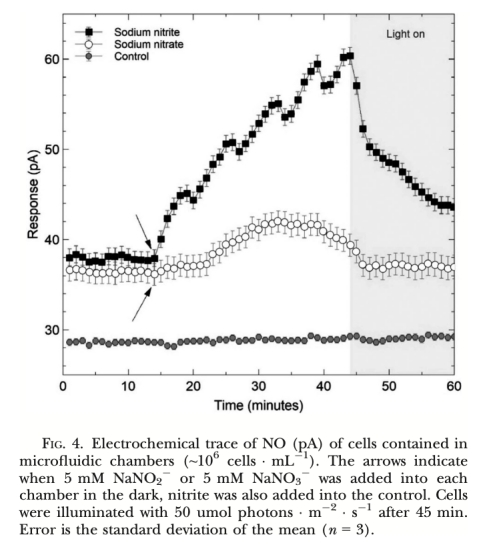
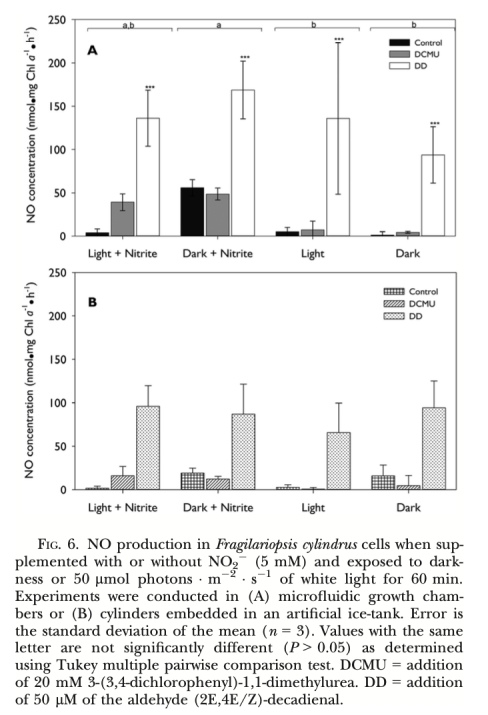
1. NO產(chǎn)生速率 (圖2, 圖3, 圖4, 圖5, 圖6, 圖7): 使用Unisense電極測量。意義: 直接量化不同處理(氮源、光照、抑制劑、溫度、鹽度)下細胞產(chǎn)生的NO量,是確定產(chǎn)生途徑和環(huán)境響應(yīng)的核心證據(jù)。圖2/圖3證明亞硝酸鹽依賴的NR途徑是主要來源;圖4/圖5/圖6證明光抑制及其與光合電子鏈的關(guān)聯(lián);圖7證明溫鹽脅迫的誘導(dǎo)作用。
2. 光合參數(shù):
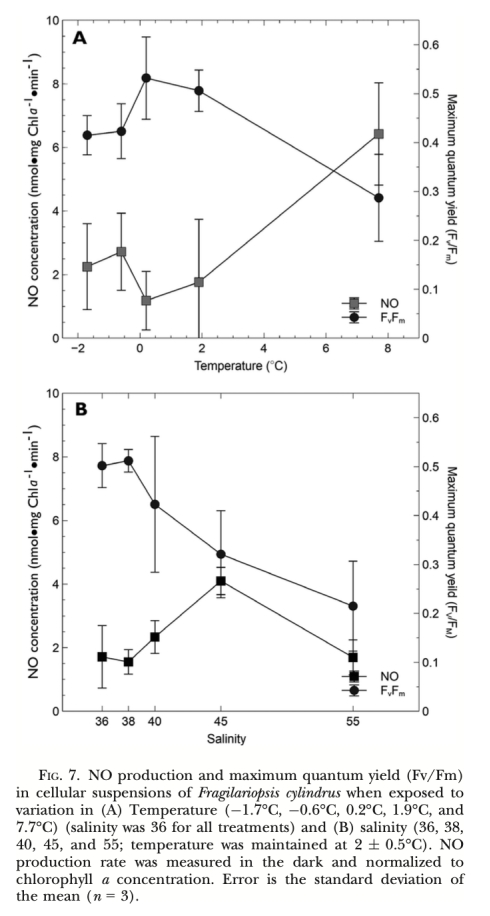
? Fv/Fm (最大量子產(chǎn)量,圖7A, 圖8A): 反映PSII最大光化學(xué)效率。意義: 指示光合機構(gòu)整體健康狀況,溫鹽脅迫(圖7A)和外源NO(圖8A)均顯著降低Fv/Fm,表明脅迫損傷。
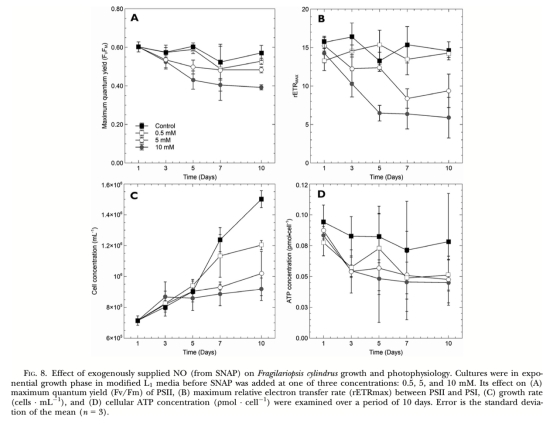
? rETRmax (最大相對電子傳遞速率,圖8B): 反映PSII到PSI的電子傳遞鏈最大能力。意義: 外源NO顯著抑制rETRmax(圖8B),表明NO干擾了光合電子傳遞。
? qP (光化學(xué)淬滅,圖9A): 反映PSII反應(yīng)中心開放程度(QA氧化態(tài))。意義: 外源NO顯著降低qP(圖9A),表明NO導(dǎo)致反應(yīng)中心“關(guān)閉”,阻礙電子從QA向QB傳遞。
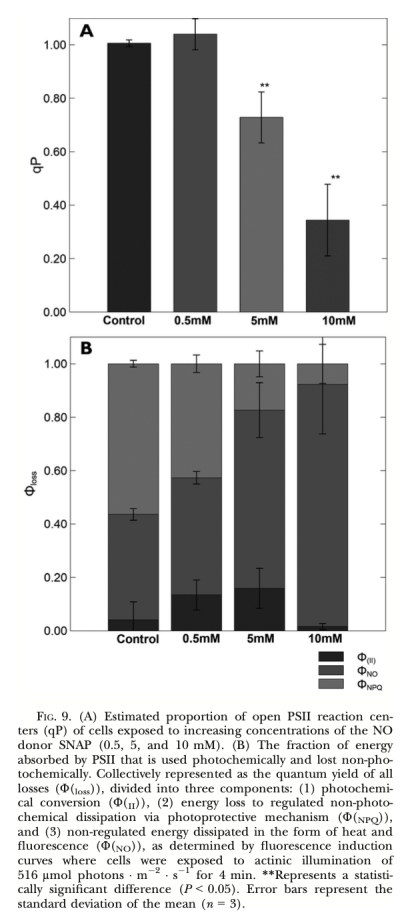
? 能量分配組分 (ΦII, ΦNPQ, ΦNO, 圖9B): 分別代表用于光化學(xué)轉(zhuǎn)化的能量、通過調(diào)節(jié)機制耗散的能量、非調(diào)節(jié)性耗散的能量。意義: 外源NO降低ΦNPQ而增加ΦNO(圖9B),表明NO破壞了依賴類胡蘿卜素/葉黃素循環(huán)的調(diào)節(jié)性能量耗散機制,導(dǎo)致更多能量以非調(diào)節(jié)性方式(可能造成損傷)耗散。
3. 生長數(shù)據(jù) (細胞濃度,圖8C): 意義: 外源NO顯著抑制藻細胞生長(圖8C),證明其對細胞增殖有毒性。
4. ATP含量 (圖8D): 意義: 高濃度外源NO(10mM SNAP)導(dǎo)致細胞ATP含量下降(圖8D),但下降程度小于光合抑制程度,提示可能存在補償機制或測量靈敏度限制。
結(jié)論
1. 產(chǎn)生機制: 柱狀脆桿藻的NO產(chǎn)生主要依賴亞硝酸鹽(NO??)途徑,由硝酸還原酶(NR) 催化。未檢測到L-精氨酸-NOS途徑的證據(jù)。光照通過維持活躍的光合電子流(促進亞硝酸鹽同化)抑制NO產(chǎn)生。光合電子傳遞受阻(如黑暗、DCMU處理、高光脅迫)導(dǎo)致亞硝酸鹽積累并觸發(fā)NR介導(dǎo)的NO產(chǎn)生。
2. 環(huán)境響應(yīng): 溫度升高(>0°C,尤其是7.7°C)和高鹽脅迫(>38)均可誘導(dǎo)NO產(chǎn)生,同時伴隨光合效率(Fv/Fm)下降,表明NO產(chǎn)生與環(huán)境脅迫密切相關(guān)。藻源醛類(DD)也能強烈誘導(dǎo)NO產(chǎn)生。
3. 生理作用: 高濃度的外源NO具有負面生理效應(yīng):抑制細胞生長、抑制PSII最大光化學(xué)效率(Fv/Fm)和電子傳遞速率(rETRmax)、導(dǎo)致PSII反應(yīng)中心關(guān)閉(qP下降)、擾亂調(diào)節(jié)性能量耗散機制(ΦNPQ下降,ΦNO上升)、降低細胞ATP水平。在脅迫條件下產(chǎn)生的內(nèi)源NO可能作為“脅迫信號”分子參與細胞生理調(diào)節(jié)或程序性死亡信號通路。
使用丹麥Unisense電極測量數(shù)據(jù)的研究意義
使用丹麥Unisense公司生產(chǎn)的NO-100μm Clarke型微電極進行測量,其研究意義至關(guān)重要且獨特:
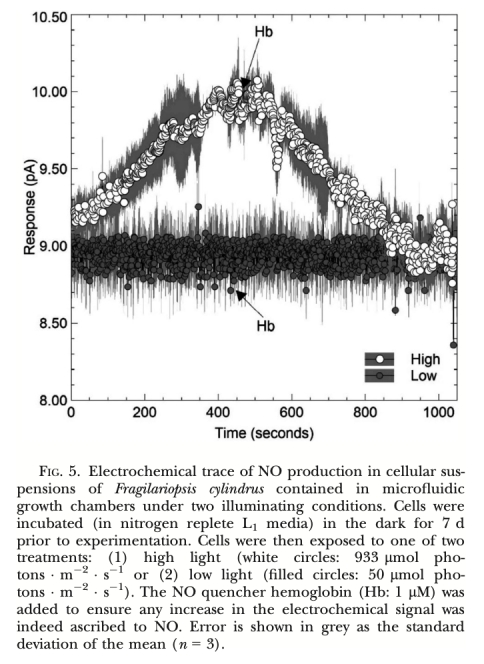
1. 實時原位高分辨率監(jiān)測: 該電極允許在微米尺度上(距離細胞約50-100μm),對活體細胞在其生長的微環(huán)境(微流體室、海冰槽模擬環(huán)境)中進行實時、連續(xù)的NO濃度變化監(jiān)測(如圖3、圖4、圖5、圖6)。這種原位監(jiān)測能力避免了傳統(tǒng)方法(如化學(xué)檢測培養(yǎng)上清液)可能帶來的樣本破壞、時間滯后和空間分辨率低的問題。
2. 驗證生化途徑的核心工具: 通過精確添加底物(如NO??)和特異性抑制劑/清除劑(如Hb),并結(jié)合電極信號的即時、顯著變化(如圖3:添加Hb后NO信號被快速淬滅;圖2:添加NO??后信號顯著升高),該技術(shù)為確定NO產(chǎn)生的主要生化途徑(亞硝酸鹽-NR途徑) 和排除其他途徑(精氨酸-NOS途徑) 提供了最直接、有力的電化學(xué)證據(jù)。其高靈敏度能可靠檢測到低至pA級別的電流變化(如圖4, 圖5)。
3. 揭示光調(diào)控動態(tài)的關(guān)鍵: 微電極能夠捕捉NO產(chǎn)生對光照狀態(tài)轉(zhuǎn)換的快速響應(yīng)(如圖4:光照開始后NO信號迅速下降)。結(jié)合光照條件的精確控制和光合抑制劑的使用(如圖6),它清晰地證明了光合電子流狀態(tài)對NO產(chǎn)生的動態(tài)開關(guān)作用(光照抑制,電子傳遞受阻則誘導(dǎo))。這在批量培養(yǎng)的化學(xué)檢測中難以實現(xiàn)如此精確的時序關(guān)聯(lián)。
4. 量化環(huán)境脅迫響應(yīng): 在模擬環(huán)境脅迫(溫度梯度、鹽度變化)實驗中(圖7),微電極能夠高靈敏度地量化不同脅迫程度下細胞產(chǎn)生的NO量。這種定量關(guān)系(如溫度升高/鹽度增加與NO產(chǎn)量上升)是建立NO作為脅迫生物標志物或信號分子假設(shè)的基礎(chǔ)數(shù)據(jù)。
5. 驗證生態(tài)相關(guān)性: 通過在海冰槽模擬環(huán)境中(圖6B)使用同款電極進行測量,雖然產(chǎn)量較低,但觀察到了與微流體室實驗一致的NO產(chǎn)生模式(如對NO??和DCMU的響應(yīng))。這提示實驗室微環(huán)境結(jié)果具有生態(tài)意義,同時微電極也揭示了不同環(huán)境(開放式vs封閉式)可能影響NO累積水平。
6. 高特異性與可靠性: 使用NO清除劑血紅蛋白(Hb)可特異性淬滅電極檢測到的信號(如圖3, 圖5),這強有力地證明了所測信號確實源于NO本身,而非其他可能的電化學(xué)干擾物質(zhì),確保了數(shù)據(jù)的可靠性和特異性。
綜上所述,丹麥Unisense NO微電極是該研究不可或缺的核心技術(shù)平臺,其高時空分辨率、特異性、靈敏度和原位監(jiān)測能力,使得研究者能夠首次在細胞微環(huán)境水平上清晰地描繪出南極硅藻柱狀脆桿藻NO產(chǎn)生的生化途徑、調(diào)控機制及其對環(huán)境脅迫的響應(yīng)動態(tài)。