熱線:021-66110810,66110819
手機:13564362870


熱線:021-66110810,66110819
手機:13564362870
Glutamate-Mediated Blood-Brain Barrier Opening: Implications for Neuroprotection and Drug Delivery
谷氨酸介導的血腦屏障開放:對神經保護和藥物遞送的意義
來源:The Journal of Neuroscience, July 20, 2016, 36(29):7727-7739
《神經科學雜志》,2016年7月20日,第36卷第29期7727-7739頁
摘要
論文摘要指出血腦屏障(BBB)功能障礙常見于多數腦部疾病,但其開放機制尚不清楚。本研究揭示了神經遞質谷氨酸在體內調節早期屏障通透性的作用。通過活體顯微鏡技術,發現反復癲癇發作及其相關的過量谷氨酸釋放,通過激活NMDA受體導致大鼠大腦皮層血管通透性增加。NMDA受體拮抗劑可減少缺血周邊腦區的屏障通透性,而使用高強度磁刺激進行神經元激活則可增加屏障通透性并促進藥物遞送。最后,一項針對惡性膠質瘤患者的雙盲臨床試驗使用對比增強磁共振成像定量評估血腦屏障通透性,證明刺激的安全性,并在15名患者中的10人身上有效增加了血腦屏障通透性。研究提出了一種雙向調節腦血管通透性的新機制。
研究目的
研究目的是探討BBB功能障礙的潛在機制,特別是檢驗過度神經元激活和細胞外谷氨酸過量積累是否導致BBB功能失調的假設。同時,研究旨在探索通過調控此機制(例如使用NMDA受體拮抗劑或經顱磁刺激)來實現對BBB通透性的雙向控制(即增加藥物遞送或防止BBB異常開放),并為神經保護和新治療策略提供臨床前和概念驗證臨床證據。
研究思路
研究思路是首先在動物模型(大鼠)中驗證核心假設。通過開窗術和活體顯微鏡技術,在麻醉大鼠大腦皮層誘導癲癇發作或直接應用谷氨酸/NMDA,實時觀察并定量分析BBB通透性(使用鈉熒光素等示蹤劑)和血管直徑的變化。研究使用藥理學工具(如NMDA受體拮抗劑D-AP-5、神經元活動阻斷劑TTX等)來探究機制,并利用探針式共聚焦激光顯微鏡檢測血管周圍鈣離子和一氧化氮信號。進一步,在光血栓中風模型中測試NMDA受體拮抗劑的保護作用,并通過經顱磁刺激(TMS)驗證神經元激活對BBB通透性的影響及其在促進藥物(如青霉素)腦遞送中的應用。最后,將發現轉化至臨床,在一項針對惡性膠質瘤患者的雙盲試驗中,使用深部經顱磁刺激(dTMS)和動態對比增強磁共振成像(DCE-MRI)評估其對BBB通透性的調節作用。
測量的數據及研究意義
1. 癲癇誘導后的血管直徑和BBB通透性變化:數據來自圖2。研究意義是直接證實癲癇活動與BBB開放相關。結果顯示癲癇發作伴隨血管直徑顯著增加(10.05±1.01%)和BBB通透性快速升高(約10分鐘后增加20.01±7.24%),意義在于建立了神經元過度興奮與BBB功能障礙的直接聯系。
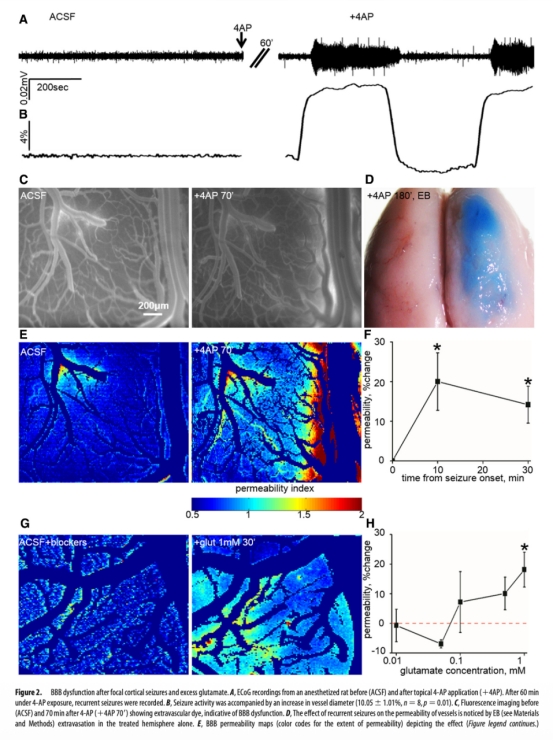
2. 谷氨酸/NMDA應用及NMDA受體拮抗劑效應下的BBB通透性:數據來自圖2G、H和圖3A。研究意義是闡明谷氨酸是通過NMDA受體介導BBB開放的關鍵分子。結果顯示局部應用谷氨酸(1mM)和NMDA均顯著增加通透性,而D-AP-5能阻斷此效應,意義在于確定了谷氨酸-NMDA受體通路是調控BBB通透性的核心機制。
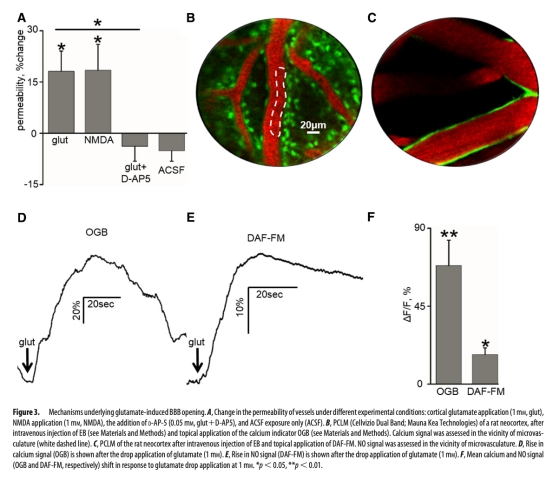
3. 谷氨酸引起的血管周圍鈣離子和一氧化氮信號變化:數據來自圖3D-F。研究意義是探討下游信號通路。結果顯示谷氨酸應用引起血管周圍鈣離子和NO水平顯著持續升高,意義在于提示鈣內流和NO生成可能是谷氨酸-NMDA受體激活導致BBB開放的細胞內信號事件。
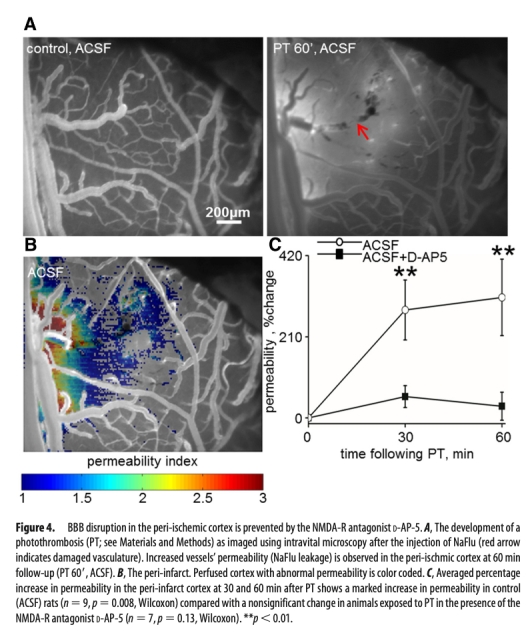
4. NMDA受體拮抗劑對中風后BBB通透性的影響:數據來自圖4。研究意義是驗證靶向此通路的治療潛力。結果顯示在光血栓模型中,D-AP-5能顯著減輕缺血周邊腦區的BBB破壞,意義在于表明NMDA受體拮抗劑或能通過保護BBB完整性發揮神經保護作用。
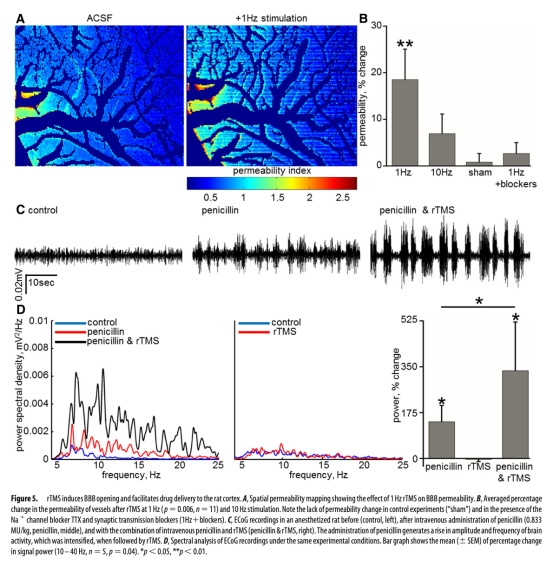
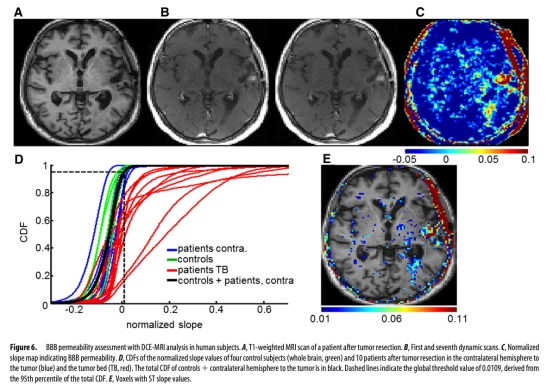
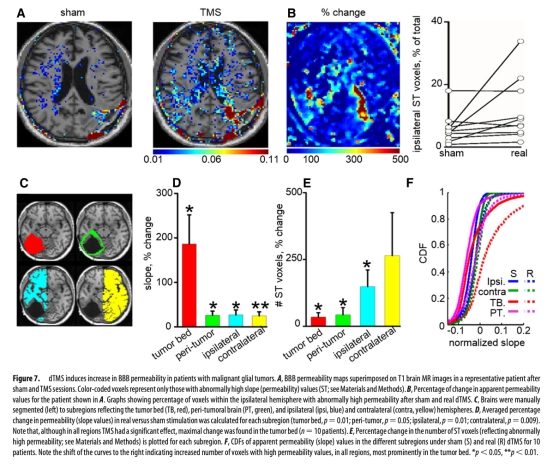
5. 經顱磁刺激(TMS)對動物和患者BBB通透性及藥物遞送的影響:數據來自圖5(動物)和圖6、7(患者)。研究意義是探索非侵入性調控BBB的方法。結果顯示1Hz rTMS能顯著增加大鼠BBB通透性并促進青霉素腦內遞送;dTMS能在多數患者中安全地增加腫瘤床及周邊腦區的BBB通透性,意義在于證明了TMS作為臨時打開BBB以增強化療遞送工具的可行性和轉化前景。
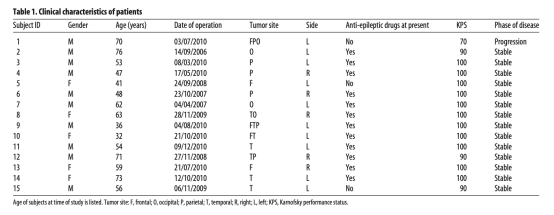
6. 患者臨床特征:數據來自表1。研究意義是描述臨床試驗人群的基本信息,為結果提供背景。
結論
研究得出結論:神經元活動釋放的過量谷氨酸通過激活腦血管內皮上的NMDA受體,引起鈣內流和一氧化氮增加,從而導致血腦屏障(BBB)通透性升高。這一機制是癲癇等相關腦病中BBB功能障礙的重要原因。靶向此通路,NMDA受體拮抗劑能減輕缺血周邊區的BBB破壞,而低頻率經顱磁刺激(TMS)能通過誘導神經元活動可控地增加BBB通透性,促進藥物向腦內遞送。臨床研究證實了深部TMS在惡性腦瘤患者中安全增加BBB通透性的潛力。因此,研究揭示了一種谷氨酸-NMDA受體依賴的BBB調控新機制,并展示了其在神經保護(通過封閉BBB)和藥物遞送(通過開放BBB)方面的雙向治療應用前景。
使用丹麥Unisense電極測量數據的研究意義
使用丹麥Unisense微電極測量組織氧分壓的數據(文中提及但未在提供的圖例中顯示具體圖表,其描述位于“Results”部分“Seizures result in BBB opening”中)顯示,在癲癇發作初期,腦組織氧分壓有短暫輕度下降,但因神經血管耦合引起的血管擴張(圖2B所示),氧分壓迅速回升并超過基線水平,隨后在發作終止后逐漸恢復正常。這一測量的研究意義在于:它直接排除了組織缺氧是癲癇活動中觀察到的BBB快速開放(約10分鐘內)的主要原因。研究意義在于為“谷氨酸-NMDA受體通路直接介導BBB開放”這一核心機制提供了關鍵的間接支持證據,將BBB開放與神經元興奮性而非繼發的缺血缺氧事件更直接地聯系起來,從而強化了研究結論的可靠性。這有助于澄清以往關于BBB開放機制的爭議,并將原因聚焦于神經遞質信號通路本身。