熱線:021-66110810,66110819
手機:13564362870


熱線:021-66110810,66110819
手機:13564362870
Divergent targets of glycolysis and oxidative phosphorylation result in additive effects of metformin and starvation in colon and breast cancer
糖酵解和氧化磷酸化的不同靶點導致二甲雙胍和饑餓在結腸癌和乳腺癌中的疊加效應
來源:Scientific Reports, volume 6, Article number: 19569, published 22 January 2016
《科學報告》,第6卷,文章編號19569,2016年1月22日發布
摘要
論文摘要指出,結合二甲雙胍(MTF)和短期饑餓(STS)能顯著損害結腸癌(CT26)和乳腺癌(4T1)的代謝和生長。饑餓引起的糖酵解通量損害被二甲雙胍通過干擾己糖激酶II活性所增強。聯合治療附加性損害氧化磷酸化:二甲雙胍幾乎廢除復合物I功能;饑餓導致OXPHOS解偶聯,并放大呼吸復合物II和IV的活性,從而結合大量ATP耗竭與活性氧顯著增加。更重要的是,聯合治療在實驗模型中深刻損害癌癥葡萄糖代謝,幾乎廢除病變生長。結果強烈表明能量代謝是減少癌癥進展的有希望靶點。
研究目的
研究目的是驗證結合二甲雙胍和短期饑餓在減少癌癥生長方面的潛力,針對結腸癌和乳腺癌模型。目標是確定這種組合如何通過靶向能量代謝的不同途徑(糖酵解和氧化磷酸化)來附加性損害癌癥能量資產,從而抑制腫瘤進展。研究旨在闡明二甲雙胍和饑餓在體內和體外對癌癥代謝、生長和存活的影響機制。
研究思路
研究思路包括體內和體外實驗。在體內,使用小鼠模型(CT26結腸癌和4T1乳腺癌),通過成像研究(如微PET掃描)評估腫瘤生長和葡萄糖代謝變化。動物分為對照組、STS組、MTF組和聯合治療組,監測腫瘤體積、葡萄糖消耗率等。在體外,使用細胞培養(CT26、4T1細胞和人類成纖維細胞作為對照),通過測量FDG攝取、酶活性、ATP濃度、氧消耗率(OCR)、活性氧(ROS)等,評估二甲雙胍和饑餓對糖酵解和氧化磷酸化的影響。方法包括蛋白質組學、Western blot、酶活性測定、免疫熒光等,以闡明機制。
測量的數據及研究意義
1 腫瘤體積生長數據:來自圖1A和1B。研究意義是顯示聯合治療能顯著抑制腫瘤生長,在兩種癌癥模型中幾乎廢除病變進展,表明靶向能量代謝的有效性。
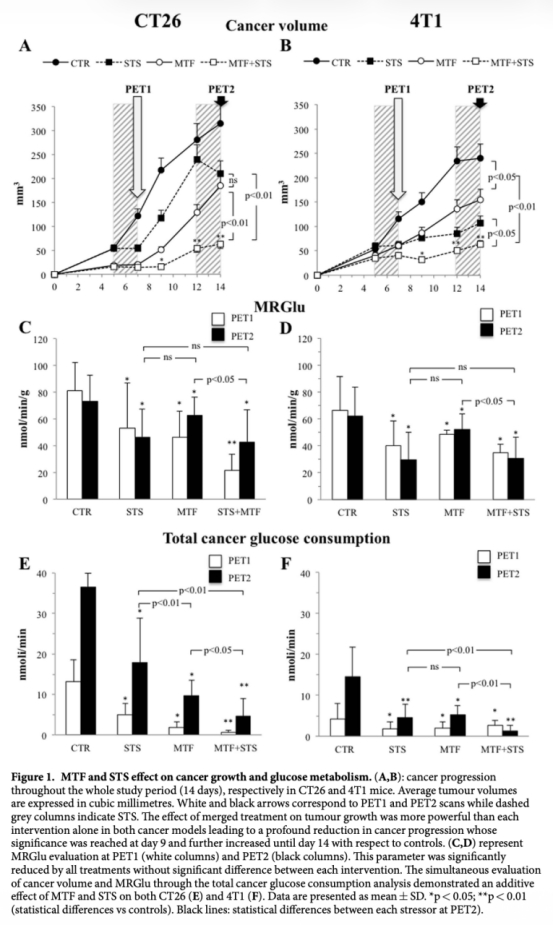
2 葡萄糖代謝率(MRGlu)和總葡萄糖消耗數據:來自圖1C、1D、1E和1F。研究意義是證明治療減少癌癥葡萄糖攝取,聯合效應附加性,表明代謝重編程被有效干擾。
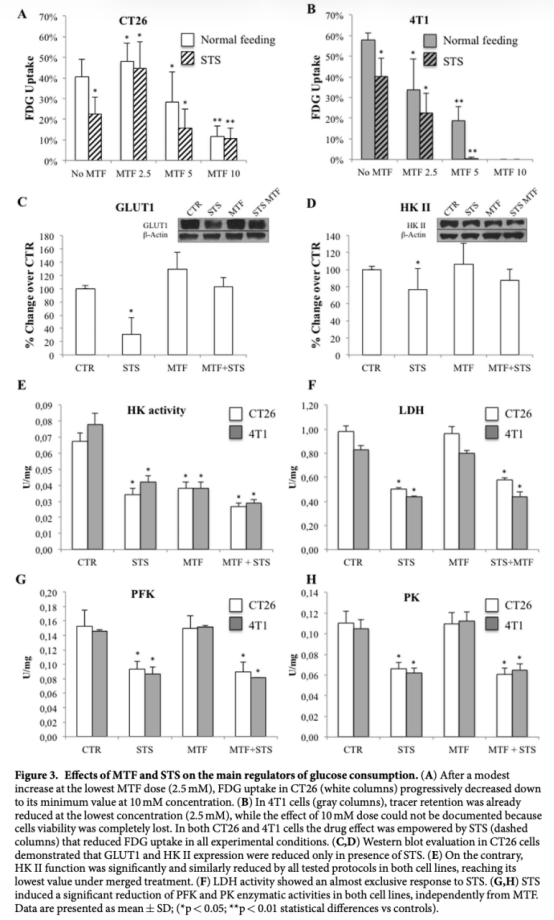
3 FDG攝取和酶活性數據(如HK、LDH、PFK、PK):來自圖3A、3B、3E、3F、3G、3H。研究意義是揭示二甲雙胍和饑餓通過不同靶點損害糖酵解,二甲雙胍抑制HK II活性,饑餓影響PFK和PK,導致葡萄糖代謝下降。
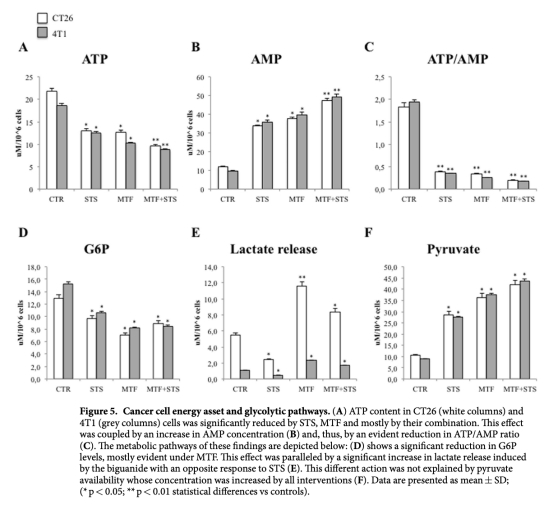
4 能量代謝數據(ATP、AMP、ATP/AMP比率):來自圖5A、5B、5C。研究意義是顯示聯合治療導致嚴重ATP耗竭,表明能量危機是抑制癌癥生長的關鍵。
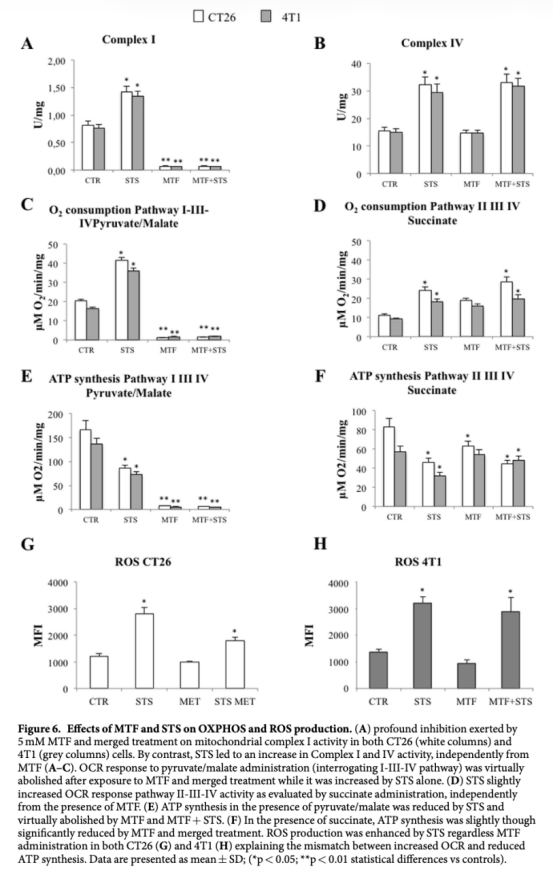
5 氧化磷酸化相關數據(復合物I和IV活性、OCR、ROS):來自圖6A、6B、6C、6D、6E、6F、6G、6H。研究意義是證明二甲雙胍抑制復合物I,饑餓解偶聯OXPHOS并增加ROS,聯合導致呼吸鏈功能嚴重受損。
6 細胞活力和增殖數據:來自圖7A、7B、7C、7D。研究意義是表明聯合治療引起細胞死亡和增殖減少,驗證其抗癌潛力。

7 信號通路數據(PI3K、pAKT、PTEN表達):來自圖7E、7F、7G。研究意義是顯示治療下調促生長通路,如PI3K-AKT,進一步解釋生長抑制機制。
結論
研究得出結論:結合二甲雙胍和短期饑餓通過靶向糖酵解和氧化磷酸化的不同途徑,附加性損害癌癥能量代謝,導致嚴重ATP耗竭、氧化損傷和生長抑制。聯合治療在體內幾乎廢除腫瘤生長,在體外引起細胞死亡和增殖減少,表明能量代謝是抗癌治療的有希望策略。這種效應在癌癥細胞中特異,正常細胞反應不同,支持其選擇性。
使用丹麥Unisense電極測量數據的研究意義
使用丹麥Unisense電極測量氧消耗率(OCR)的數據(如Fig. 6C, 6D)具有關鍵研究意義。Unisense電極是一種高靈敏度的安培法氧傳感器,用于直接量化組織氧分壓(PO2)和氧化代謝變化。在研究中,它被用于測量細胞培養中的OCR,以評估二甲雙胍和饑餓對線粒體呼吸鏈功能的影響。數據顯示,二甲雙胍幾乎廢除通過復合物I-III-IV途徑的OCR,而饑餓增加OCR但導致OXPHOS解偶聯。這些測量直接證明了治療對氧化磷酸化的干擾:二甲雙胍通過抑制復合物I減少氧消耗,饑餓則增加氧消耗但降低ATP合成效率,導致ROS增加。Unisense電極的高精度和實時監測能力使得能夠區分不同呼吸途徑的貢獻,從而闡明聯合治療如何附加性損害能量代謝。這不僅驗證了代謝靶點的有效性,還為開發基于能量代謝的抗癌策略提供了可靠的工具支持。