熱線:021-66110810,66110819
手機:13564362870


熱線:021-66110810,66110819
手機:13564362870
Mitigation in Multiple Effects of Graphene Oxide Toxicity in Zebrafish Embryogenesis Driven by Humic Acid
(EST)氧化石墨烯對于腐殖酸驅動的斑馬魚胚胎毒性的緩解作用
來源:Environ. Sci. Technol. 2015, 49, 10147?10154
論文摘要
這篇論文研究了天然有機質(NOM)的主要成分——腐殖酸(HA)如何影響氧化石墨烯(GO)對斑馬魚胚胎的毒性。研究發現,GO會附著在胚胎絨毛膜上,造成物理屏障導致缺氧,并誘發氧化應激,從而導致孵化延遲和心臟水腫等毒性效應。而HA通過與GO結合,改變了GO的表面形態和電荷,顯著減輕了這些毒性作用,揭示了HA在自然水體中作為GO“天然解毒劑”的潛力,提示在評估GO的環境風險時必須考慮NOM的存在。
研究目的
本研究旨在探究一個尚未被充分研究的領域:廣泛存在于自然水體中的腐殖酸(HA)如何改變氧化石墨烯(GO)對水生脊椎動物(以斑馬魚胚胎為模型)的毒性效應及其內在機制。
研究思路
研究采用多層次的毒性評估方法,思路清晰:
表征與相互作用:首先,對GO、HA以及兩者結合形成的GO-HA復合物進行物理化學表征(如形貌、尺寸、表面電荷、化學結構等),確認HA成功修飾了GO。
毒性表型觀察:在斑馬魚胚胎模型中,分別設置對照組、HA單獨暴露組、GO單獨暴露組和GO-HA共同暴露組,觀察并記錄胚胎孵化率、心包水腫發生率、心跳速率等發育毒性指標。
機制深入探究:
界面相互作用:研究GO或GO-HA與胚胎第一道屏障——絨毛膜之間的相互作用,包括附著程度、對絨毛膜表面結構和蛋白二級結構的影響。
攝取與轉運:觀察GO或GO-HA如何進入胚胎以及在胚胎內的分布位置。
細胞與分子水平效應:檢測線粒體損傷、氧化應激水平(如活性氧ROS、抗氧化酶活性)、以及脂質、蛋白質和DNA的氧化損傷標志物。
測量的數據、意義及來源
研究測量了多方面的數據來支持其結論,具體如下:
發育毒性數據:測量了孵化率、心包水腫發生率和心跳速率。這些數據直接證明了GO的發育毒性以及HA的緩解作用。其意義在于 提供了最直觀的毒性證據。數據主要來自文本描述(如:GO100暴露組孵化率降至37.0±5.0%,而GO-HA組恢復至70.0±8.0%),支持信息中的圖S4-S6可能提供了詳細數據。
絨毛膜-納米材料相互作用數據:
相互作用界面比例:通過TEM圖像分析得出,GO與絨毛膜的相互作用界面高達86.7%,而GO-HA降至26.4%。
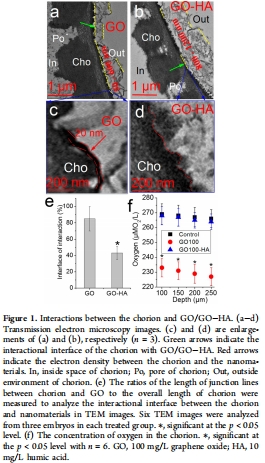
絨毛膜突起數量:GO暴露導致絨毛膜突起數量減少至對照的42.0%,而GO-HA組恢復至84.2%。
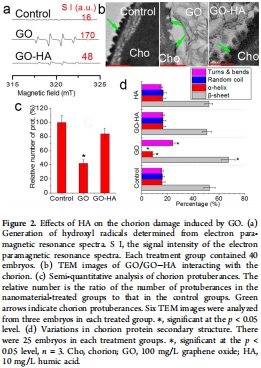
研究意義:這些數據揭示了GO毒性的一個關鍵物理機制——通過緊密包裹胚胎造成物理性窒息和機械損傷,而HA通過減少這種相互作用起到了保護作用。
使用丹麥Unisense微電極測量的氧濃度數據:
數據內容:使用Unisense氧微傳感器測量了絨毛膜內部空間的氧氣濃度。結果顯示,GO暴露組胚胎的絨毛膜內氧氣濃度顯著降低(在250μm深度處為227μM),而對照組和GO-HA組則保持正常水平(約266-264μM)。
詳細解讀與研究意義:
技術優勢:Unisense微電極是一種高空間分辨率的傳感器,能夠無損地、實時地測量微環境(如單個胚胎絨毛膜腔)中的溶解氧濃度。這對于研究納米材料引起的局部物理性缺氧至關重要,是傳統生化方法無法替代的。
核心發現:該數據直接證實了GO的包裹行為導致了胚胎局部“缺氧”微環境的形成。缺氧是解釋GO毒性(如孵化延遲、發育畸形)的一個關鍵因素,因為胚胎發育高度依賴氧氣。
機制驗證:該測量結果與TEM觀察到的GO緊密包裹絨毛膜的現象(圖1a, c)完美吻合,將形態學觀察(因)與功能性后果(果)直接聯系起來,強有力地支持了“物理屏障致缺氧”的毒性機制。
解毒證據:GO-HA組的氧濃度恢復正常,直觀地證明了HA通過減少GO的包裹,有效緩解了缺氧壓力,這是HA解毒作用的一個直接且定量的證據。
氧化應激與損傷數據:
羥基自由基(·OH):通過電子順磁共振(EPR)測量,GO暴露組·OH信號增強,HA使其減弱。意義:證明GO能誘發氧化應激,HA可緩解。
生化指標:測量了超氧化物歧化酶(SOD)活性、谷胱甘肽(GSH)和丙二醛(MDA)含量、ROS熒光強度等。意義:從酶活性和代謝產物水平證實GO導致氧化損傷,HA起到保護作用。數據來自文本和圖S14-S16。
分子損傷標志物:測量了蛋白質羰基化和8-羥基脫氧鳥苷(8-OHdG)含量。意義:直接證明了GO造成了蛋白質和DNA的氧化損傷,HA減輕了此損傷。
納米材料表征數據:通過TEM、AFM、拉曼光譜、Zeta電位等證實HA成功附著在GO上,使其邊緣變得平滑,表面負電荷增加,分散性更好,更穩定。
研究結論
本論文得出以下核心結論:
HA對GO的解毒作用:HA能顯著緩解GO對斑馬魚胚胎的發育毒性(孵化延遲、心包水腫等)。
解毒機制:
物理修飾:HA通過π-π相互作用吸附在GO表面,改變其形貌,使其邊緣變平滑,并增加其表面負電荷和分散穩定性。
減少初始相互作用:修飾后的GO-HA與胚胎絨毛膜的相互作用顯著減弱,避免了對絨毛膜的物理包裹和損傷,防止了局部缺氧環境的形成。
影響攝取與分布:HA改變了GO在胚胎內的攝取途徑和分布,使其更多停留在保護性的表層細胞,而非重要的深層組織和卵黃細胞。
緩解下游毒性:上述作用最終導致GO誘導的線粒體損傷、氧化應激以及對生物大分子(脂質、蛋白質、DNA)的損傷均得到顯著緩解。
環境意義:由于HA在自然水體中廣泛存在,它在評估GO的實際環境風險時扮演著“天然解毒劑”的角色。因此,在實驗室中使用純GO進行的毒性研究可能會高估其在真實環境中的風險。