熱線:021-66110810,66110819
手機:13564362870


熱線:021-66110810,66110819
手機:13564362870
Intermittent hypoxia alters gut microbiota diversity in a mouse model of sleep apnoea
間歇性低氧改變腸道菌群
來源:Eur Respir J 2015; 45: 1055–1065
論文摘要
本研究評估了模擬阻塞性睡眠呼吸暫停(OSA)核心特征之一的間歇性低氧是否會改變小鼠模型的糞便微生物組。通過測量結腸糞便中的氧分壓(PaO2)并分析微生物組組成,研究發現間歇性低氧在腸道近上皮區域(<200μm)引發了低氧/再氧合事件,導致微生物組全局結構改變,包括α-多樣性(Shannon指數)增加和β-多樣性變化。具體而言,間歇性低氧暴露組小鼠的厚壁菌門(Firmicutes)豐度增加,而擬桿菌門(Bacteroidetes)和變形菌門(Proteobacteria)豐度減少。這表明間歇性低氧可能通過改變腸道微生物組,影響OSA相關的生理互作。
研究目的
本研究旨在探究間歇性低氧(模擬OSA的典型生理刺激)是否會導致腸道微生物組多樣性和組成的改變。OSA與代謝紊亂(如肥胖)密切相關,但間歇性低氧對腸道微生物組的影響尚未被研究。研究假設間歇性低氧會引起腸道微環境氧分壓波動,進而改變微生物群落。
研究思路
研究采用兩步實驗設計:
驗證氧分壓波動:首先在麻醉小鼠中,使用Unisense氧微電極直接測量小腸糞便中的PaO2,確認間歇性低氧能否在腸道近上皮區域(<200μm范圍內)產生低氧/再氧合波動。
分析微生物組變化:將小鼠分為兩組——間歇性低氧暴露組(模擬嚴重OSA,6周內每天6小時間歇低氧)和常氧對照組。6周后收集糞便樣本,通過16S rRNA焦磷酸測序和QIIME生物信息學分析,比較微生物組的α-多樣性(如Shannon指數)、β-多樣性(如ANOSIM分析)以及門、科、屬水平的相對豐度。
測量的數據、研究意義及圖表來源
研究測量了多類數據,以下按類別說明其意義和來源:
腸道氧分壓(PaO2)數據:
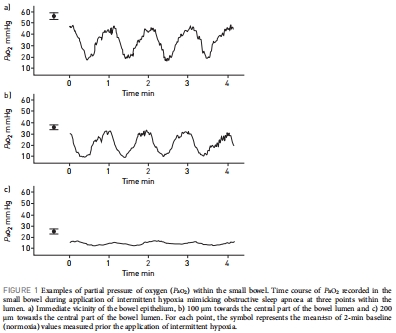
數據內容:使用Unisense電極測量小腸糞便中不同位置(近上皮、100μm、200μm處)的PaO2,顯示間歇性低氧導致PaO2出現波動性下降,振幅隨距離上皮越遠而減小。
研究意義:直接證實間歇性低氧能穿透腸道微環境,造成微生物棲息地的氧波動,為微生物組變化提供物理機制證據。這些波動可能影響好氧/厭氧菌的生態平衡。
數據來源:來自圖1(圖中展示了PaO2隨時間變化的曲線,包括基線常氧和間歇性低氧下的記錄)。
體重變化數據:
數據內容:測量小鼠基線體重和6周后體重,時間因素對體重增加有顯著影響,但間歇性低氧與常氧組間無顯著差異。
研究意義:排除體重變化作為微生物組改變的混淆因素,突出間歇性低氧的直接作用。
數據來源:來自文本結果部分的“Change in body weight”段落。
微生物組多樣性數據:
α-多樣性:如Shannon指數(測量物種均勻度)和Chao1指數(測量物種豐富度)。間歇性低氧組Shannon指數顯著高于常氧組,表明多樣性增加。
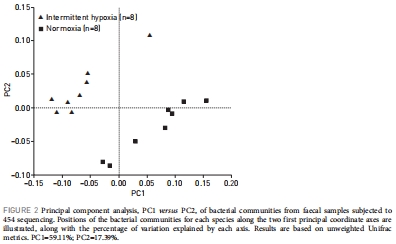
β-多樣性:通過主成分分析(PCA)和ANOSIM檢驗顯示兩組微生物群落結構顯著分離。
研究意義:表明間歇性低氧不僅增加微生物組內物種均勻度,還改變整體群落結構,可能增強微生物組對氧應激的適應性。
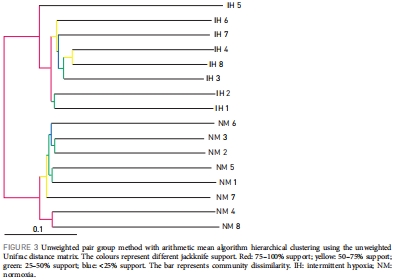
數據來源:Shannon和Chao1指數來自表1;PCA結果來自圖2;ANOSIM和聚類分析來自圖3。
微生物組成豐度數據:
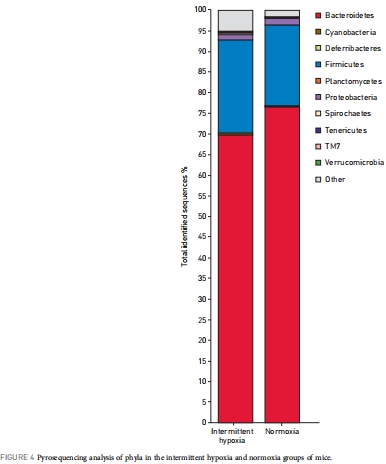
門水平:擬桿菌門、厚壁菌門和變形菌門的相對豐度變化(無顯著差異,但趨勢改變)。
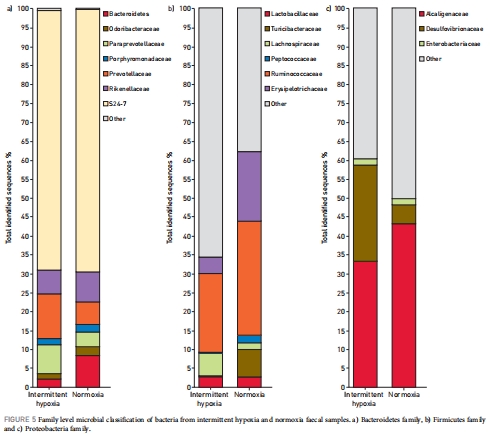
科和屬水平:間歇性低氧組中,普雷沃菌科(Prevotellaceae)、副普雷沃菌科(Paraprevotellaceae)和毛螺菌科(Lachnospiraceae)豐度顯著增加,而擬桿菌科(Bacteroidaceae)和丹毒絲菌科(Erysipelotrichaceae)等減少。
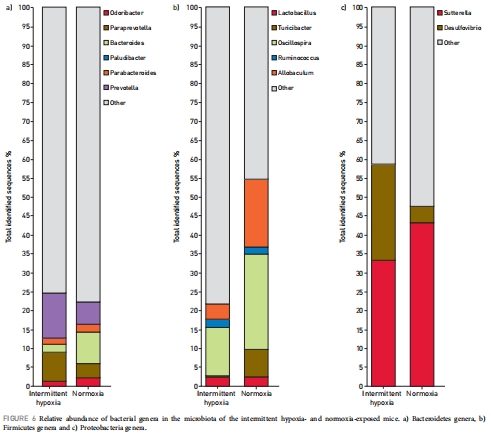
研究意義:特定菌群變化(如Prevotella和Desulfovibrio增加)提示間歇性低氧可能促進黏液降解和硫酸鹽還原,潛在影響腸道屏障功能和代謝疾病風險。
數據來源:門水平數據來自圖4;科水平數據來自圖5;屬水平數據來自圖6。
研究結論
本研究得出以下核心結論:
間歇性低氧(模擬OSA)確實能在腸道近上皮區域(<200μm)引起氧分壓波動,直接改變微生物組的微環境。
間歇性低氧顯著增加腸道微生物組的α-多樣性(如Shannon指數),并改變β-多樣性,導致微生物群落結構重組。
在科和屬水平上,間歇性低氧促進厭氧菌(如Prevotella和Desulfovibrio)增殖,可能破壞宿主-微生物組穩態,增加腸道通透性和系統炎癥風險。
這些發現提示,OSA患者的腸道微生物組可能因間歇性低氧而失調,進而參與OSA相關的代謝并發癥。
詳細解讀使用丹麥Unisense電極測量數據的研究意義
使用丹麥Unisense氧微電極測量的PaO2數據是本研究的關鍵創新點,其研究意義可詳細解讀如下:
技術獨特性:Unisense電極是一種高靈敏度、快響應(90%響應時間<2秒)的極譜氧傳感器,直徑僅50μm,能無損插入腸道糞便微環境,直接測量不同深度的實時氧分壓。這種空間分辨率(可精確到μm級)是傳統方法無法實現的,避免了樣本破壞或間接推斷的誤差。
機制驗證意義:數據來自圖1,顯示在間歇性低氧暴露下,近上皮區域(0-200μm)的PaO2出現明顯波動(振幅隨距離增大而衰減),這直接證實了研究假設——OSA相關的動脈血氧飽和度波動能通過擴散影響腸道微生物棲息地。理論計算(基于Fick擴散定律)支持該數據,表明在200μm處氧波動振幅仍達36%,暗示大量微生物會感知氧變化。
生態學意義:氧波動創造了動態氧化還原梯度,賦予厭氧菌(如Prevotella)選擇優勢,而好氧菌受抑制。這解釋了微生物組多樣性增加和群落變化,凸顯了物理微環境對微生物生態的直接驅動作用。
臨床延伸意義:該測量為OSA與腸道疾病(如代謝綜合征)的關聯提供了機制橋梁。例如,氧波動可能削弱腸道屏障,導致內毒素易位,引發系統炎癥。這啟示未來研究可針對OSA患者進行類似微生物組干預。
綜上,Unisense電極數據不僅驗證了間歇性低氧的物理傳遞鏈條,還為理解OSA多器官影響提供了新視角,強調微環境測量在宿主-微生物研究中的重要性。