熱線:021-66110810,66110819
手機(jī):13564362870


熱線:021-66110810,66110819
手機(jī):13564362870
研究簡介:大腦雖然只占體重2%,卻消耗了近20%的靜息能量,其ATP幾乎全部由葡萄糖有氧氧化供給。幾十年來,神經(jīng)代謝領(lǐng)域卻流傳著一個看似矛盾的假設(shè):當(dāng)神經(jīng)元突然高頻放電時,第一時間并不動用“主發(fā)電機(jī)”——線粒體氧化磷酸化,而是先啟動“應(yīng)急電池”——糖酵解,尤其是在星形膠質(zhì)細(xì)胞內(nèi)的糖酵解。本研究利用大鼠海馬腦片,結(jié)合氧微電極記錄、NADH熒光成像及數(shù)學(xué)建模,系統(tǒng)評估了神經(jīng)元活動瞬間的能量來源。傳統(tǒng)觀點(diǎn)認(rèn)為,神經(jīng)活動首先由糖酵解(主要在星形膠質(zhì)細(xì)胞)供能,再通過乳酸轉(zhuǎn)運(yùn)給神經(jīng)元進(jìn)行氧化磷酸化。研究卻發(fā)現(xiàn)在阻斷乳酸脫氫酶(LDH)、或僅用20%O?模擬生理低氧條件下,神經(jīng)元刺激仍迅速降低胞外O?和胞內(nèi)NADH,提示氧化磷酸化被立即動員.藥理學(xué)逐步阻斷突觸前動作電位、Ca2?內(nèi)流-遞質(zhì)釋放、突觸后谷氨酸受體電流及動作電位,可分別減少11%、17%、46%、26%的O?消耗,證明這些關(guān)鍵信息處理環(huán)節(jié)均由氧化磷酸化直接供能.阻斷LDH后,活動誘發(fā)的O?與NADH變化幅度不變,否定了星形膠質(zhì)細(xì)胞-神經(jīng)元乳酸穿梭假說對瞬時能量供給的必要性。該工作顛覆了“先糖酵解后氧化”的傳統(tǒng)教條,明確了大腦信息處理主要由氧化磷酸化實時驅(qū)動,為理解腦能量代謝及fMRI信號生理基礎(chǔ)提供直接證據(jù)。
Unisense微電極系統(tǒng)的應(yīng)用
使用了Unisense Clark型玻璃氧微電極,尖端直徑10μm。實現(xiàn)了原位測量海馬切片內(nèi)胞外氧濃度變化,作為氧化磷酸化速率的直接指標(biāo)。微電極尖端定位于CA1輻射層距錐體細(xì)胞層30μm、距切片表面約100μm處。通過Clark型玻璃微電極實現(xiàn)10μm空間分辨率,實時監(jiān)測刺激誘發(fā)的O?濃度動態(tài)變化。量化不同藥物(如NBQX、Cd2?)對O?消耗的抑制比例(如突觸后機(jī)制占72%),為能量分配提供實驗依據(jù)。
實驗結(jié)論
研究通過海馬腦片多手段實驗,首次直接證明神經(jīng)元活動瞬間所需ATP主要由氧化磷酸化即時提供,而非傳統(tǒng)認(rèn)為的“先糖酵解后氧化”或星形膠質(zhì)細(xì)胞-神經(jīng)元乳酸穿梭模式。阻斷乳酸脫氫酶或降低氧濃度后,神經(jīng)元刺激仍迅速耗氧并降低NADH,表明氧化磷酸化被立即動員,承擔(dān)≥62%的ATP增量。利用藥理-建模拆分,11%的氧耗用于突觸前動作電位,17%用于Ca2?內(nèi)流-遞質(zhì)釋放,46%用于突觸后谷氨酸受體電流,26%用于突觸后動作電位。抑制LDH不改變刺激誘發(fā)的氧耗與NADH變化,否定了星形膠質(zhì)細(xì)胞產(chǎn)乳酸快速供神經(jīng)元氧化磷酸化的必要性。
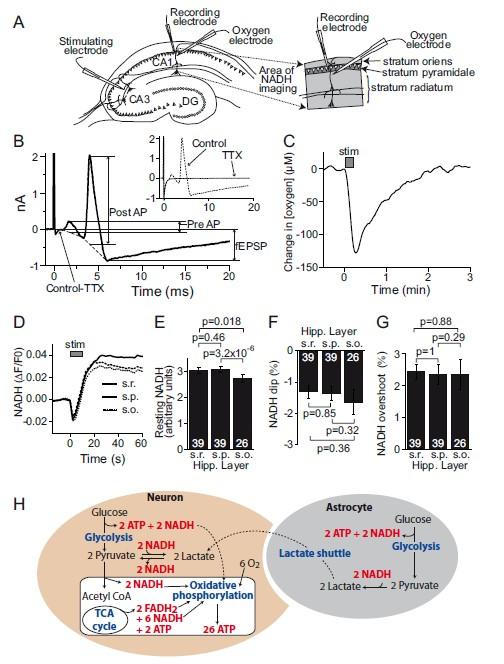
圖1、刺激誘發(fā)的場電位及O?與NADH變化。A圖:實驗電極位置及成像區(qū)域示意圖。B圖:左上小圖:0.33 Hz刺激下記錄的場電位(含突觸前動作電位、場興奮性突觸后電位fEPSP及突觸后群體峰電位),TTX阻斷后僅保留刺激偽跡。主圖:TTX阻斷前后的差值曲線,顯示各成分測量方法(突觸前動作電位幅度、fEPSP斜率、群體峰電位幅度)。C圖:20 Hz刺激10秒誘發(fā)細(xì)胞外[O?]下降(均值118±8μM)。D圖:NADH熒光雙相響應(yīng)(初始下降1.4%,后續(xù)超調(diào)2.4%),在輻射層(s.r.)、錐體層(s.p.)和腔隙層(s.o.)無顯著差異。E-G圖:各層NADH靜息熒光(E)、刺激誘發(fā)的NADH下降(F)及超調(diào)(G)的定量比較。H圖:糖酵解、TCA循環(huán)與氧化磷酸化對NADH水平的調(diào)控機(jī)制示意圖。
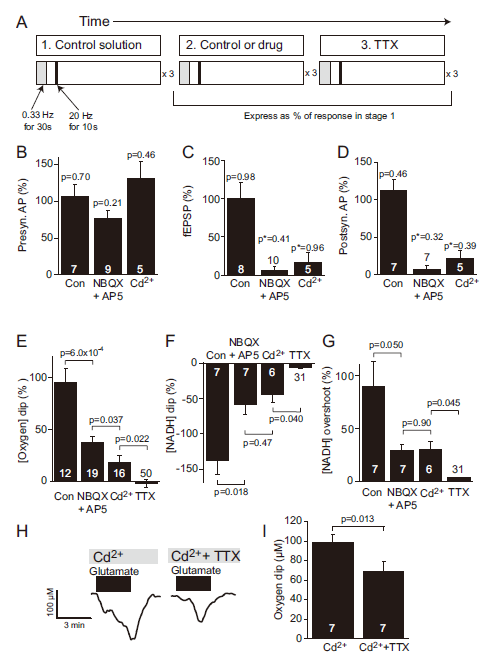
圖2、不同亞細(xì)胞機(jī)制的O?消耗藥理學(xué)分析。A圖:實驗流程設(shè)計(三階段刺激協(xié)議,含藥物干預(yù))。B-D圖:NBQX+AP5(阻斷突觸后電流)選擇性抑制fEPSP和群體峰電位,對突觸前動作電位無影響。Cd2?阻斷突觸傳遞但保留突觸前動作電位,TTX阻斷全部電活動。E-G圖:逐步阻斷突觸后活動(NBQX+AP5)、遞質(zhì)釋放(Cd2?)及全部活動(TTX)使[O?]下降依次減少63%、82%和100%。NADH下降及超調(diào)呈現(xiàn)類似階梯式抑制。H-I圖:谷氨酸(500μM)在Cd2?存在下誘發(fā)的[O?]下降,TTX進(jìn)一步減少29%,表明動作電位消耗O?
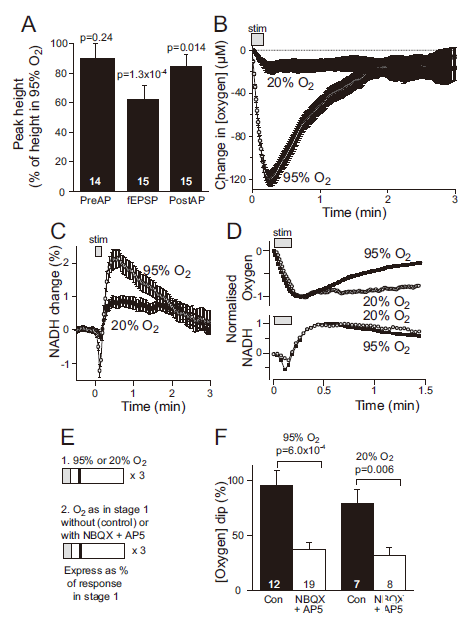
圖3、生理O?水平下氧化磷酸化支持神經(jīng)活動。A圖:20%O?灌流降低fEPSP(38%)和群體峰電位5%),但不影響突觸前動作電位。B圖:20%O?下[O?]下降幅度減小但持續(xù)時間延長(恢復(fù)需5分鐘)。C圖:NADH初始下降及超調(diào)幅度在低O?下降低。D圖:標(biāo)準(zhǔn)化后的O?下降與NADH超調(diào)時間重疊。E-F圖:NBQX+AP5在95%和20%O?下對[O?]下降的抑制比例無差異(63%vs.68%),表明突觸后O?消耗與O?水平無關(guān)。
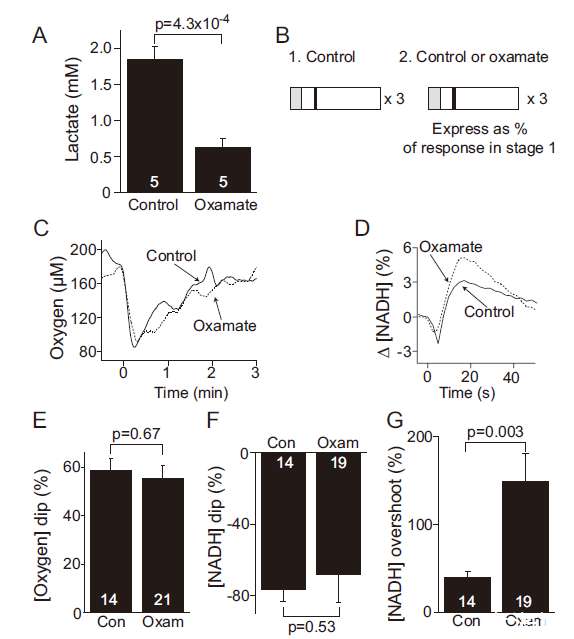
圖4、LDH阻斷不影響O?與NADH初始下降。A圖:LDH抑制劑草酸鹽使細(xì)胞外乳酸減少66%。B圖:實驗設(shè)計(階段2加入oxamate)。C-D圖:oxamate不改變[O?]下降(E)和NADH初始下降(F),但增加NADH超調(diào)(G)(p=0.003),提示糖酵解延遲激活。
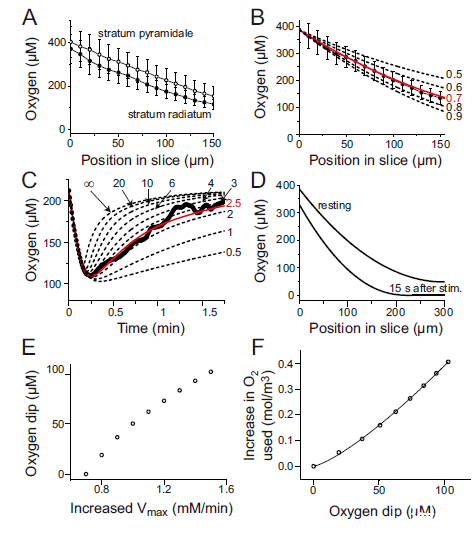
圖5、巨噬細(xì)胞復(fù)極化的機(jī)制研究。a)接受不同處理的RAW 264.7細(xì)胞的RNA測序分析示意圖。該圖由Figdraw創(chuàng)建。b)來自不同群體的RAW 264.7細(xì)胞基因的PCA分析。數(shù)據(jù)按原樣顯示(N=3)。c)來自不同組的RAW 264.7細(xì)胞轉(zhuǎn)錄組中差異表達(dá)基因的基因聚集。數(shù)據(jù)按原樣顯示,并按平均值顯示(N=3)。d)來自不同組的RAW 264.7細(xì)胞的炎癥相關(guān)途徑中涉及的DEGs的熱圖分布。數(shù)據(jù)按原樣顯示(N=3)。e)LPS/IFN-γ和LPS/IFN-γ+CSN處理的RAW 264.7細(xì)胞轉(zhuǎn)錄組中DEGs的火山圖。f)LPS/IFN-γ和LPS/IFN-γ+CSN處理細(xì)胞的前15個DEGs的相互作用。g)LPS/IFN-γ和LPS/IFN-γ+CSN處理細(xì)胞的KEGG富集分析氣泡圖h)Nfkb2的mRNA表達(dá),來自不同組的RAW 264.7細(xì)胞的Mapk12和Tnf。數(shù)據(jù)表示為SD±均值(N=3)。i)IL-17信號通路的GSEA圖顯示,用LPS/IFN-γ處理的RAW 264.7細(xì)胞CSN處理后顯著下調(diào)(NES=-1.74)。j)CSN巨噬細(xì)胞復(fù)極化的分子機(jī)制示意圖。k)來自不同組的RAW 264.7細(xì)胞的p65、p38和FosB的蛋白質(zhì)印跡分析。
結(jié)論與展望
本研究研究了大腦信息處理過程中能量供應(yīng)的核心機(jī)制,挑戰(zhàn)了"神經(jīng)元活動初期依賴糖酵解供能"的傳統(tǒng)觀點(diǎn)。通過海馬體切片實驗,研究人員驗證了氧化磷酸化(而非糖酵解)是突觸前動作電位、神經(jīng)遞質(zhì)釋放、突觸后電流和動作電位等關(guān)鍵神經(jīng)活動的主要能量來源。本研究首次整合Unisense O?電極、NADH成像和場電位記錄,實現(xiàn)多參數(shù)代謝-電活動同步分析。通過Clark型玻璃微電極實現(xiàn)10μm空間分辨率,實時監(jiān)測刺激誘發(fā)的O?濃度動態(tài)變化。這一發(fā)現(xiàn)對理解腦功能成像(如BOLD信號)的生理基礎(chǔ)具有重要意義。本顛覆了“糖酵解先供能”的傳統(tǒng)教條,為理解大腦信息處理的能量供應(yīng)機(jī)制、解釋BOLD-fMRI信號生理基礎(chǔ)提供了直接實驗依據(jù)。
 相關(guān)新聞
相關(guān)新聞