熱線:021-66110810,66110819
手機:13564362870


熱線:021-66110810,66110819
手機:13564362870
研究簡介:結直腸癌傳統療法存在系統毒性和療效不足的挑戰。新興證據表明,分子氫(H?)可通過抑制增殖和誘導“腫瘤休眠”表型(以細胞周期阻滯和代謝靜息為特征)來發揮抗腫瘤作用。基于此,本研究設計的PMA納米系統能夠在650納米激光照射下,利用腫瘤微環境中富含的乳酸和谷胱甘肽(GSH)作為犧牲劑,通過光催化水分解反應實現時空可控的H?生成。本論文報道了一種針對結直腸癌的新型納米治療策略。該研究通過構建一種鉑摻雜的單原子金屬有機框架(PM),并將其與抗炎藥物5-氨基水楊酸(5-ASA)結合形成PMA納米平臺,實現了光控產氫誘導腫瘤休眠與催化活性氧(ROS)風暴殺傷的雙重治療模式。生成的H?與釋放的5-ASA協同抑制NF-κB信號通路,從而將腫瘤從增殖狀態轉變為對氧化還原敏感的“休眠”狀態。這種休眠狀態使腫瘤細胞更容易受到后續治療的攻擊。
在初次光照約8小時后,納米材料在腫瘤微環境中降解并釋放出光敏劑原卟啉。此時進行第二次激光照射,可引發強烈的ROS爆發,選擇性清除已處于脆弱狀態的休眠腫瘤細胞,實現催化治療。研究團隊通過系統的材料表征(如TEM、XPS、XRD)驗證了PMA的成功合成與穩定性。體外和體內實驗表明,該平臺具有良好的生物相容性和高效的H?生成能力。在CT-26荷瘤小鼠模型中,PMA聯合雙次光照治療方案顯示出顯著的抗腫瘤效果,腫瘤體積減少約90%,并有效重塑了免疫抑制性腫瘤微環境。機制研究表明,H?通過調節ACLY、CKS2、CDC34、CDK7和c-MYC等關鍵細胞周期蛋白,誘導了持續的增殖停滯。本論文研究將單原子催化劑用于精準催化H?生成,并與免疫調節相結合,提出了一種通過協調細胞周期控制和微環境重編程來攔截腫瘤進展的新框架,為結直腸癌的精準催化治療提供了新范式。
Unisense微電極分析系統的應用
利用Unisense微電極對PMA納米顆粒的產氫過程進行了精確的定量分析,在體外實驗中,研究人員將PMA納米顆粒與作為犧牲劑的乳酸或谷胱甘肽(GSH)共同孵育,并用650納米激光照射。同時,將Unisense氫微電極插入反應體系,每秒自動記錄一次氫濃度的變化。這種方法直接證實了PMA能夠利用腫瘤微環境中的內源性物質有效地產氫,并精確繪制了產氫動力學曲線。在動物模型(攜帶CT-26腫瘤的BALB/c小鼠)中,Unisense微電極的應用更為關鍵。研究人員通過尾靜脈或瘤內注射PMA后,將小鼠麻醉,將氫微電極直接插入腫瘤組織內部。通過這種原位、在體的檢測方式,他們成功實現了對活體腫瘤局部H?濃度的實時監控,并記錄了在固定時間點(如注射后0、2、4、8小時)的氫濃度變化。
實驗結論
實驗結果表明,H2通過抑制NF-κB信號通路誘導腫瘤休眠,在結直腸癌中展現出治療潛力,從而帶來了新的治療前景。將可見光激活的SACs與5-氨基水楊酸結合,用于H2生成,協同觸發腫瘤凋亡并重塑腫瘤微環境,實現強效的腫瘤生長抑制。通過氧化還原調節,PMA緩解T細胞耗盡,增強腫瘤免疫抑制,有效抑制惡性增殖。從機制上看,H2可能通過線粒體內膜重塑和增殖相關激酶的調控來協調氧化還原穩態。在BALB/c小鼠模型中,PMA給藥顯著減少腫瘤體積(對照組90%,p<0.0001),并增強腫瘤細胞凋亡,驗證其治療效果。這一基于SAC的策略為結直腸癌管理建立了新范式,通過氫氣療法和SACs協調調節腫瘤微環境動態和免疫反應,實現腫瘤增生的雙重抑制和選擇性誘導凋亡,為精準腫瘤學開辟了變革性方法。
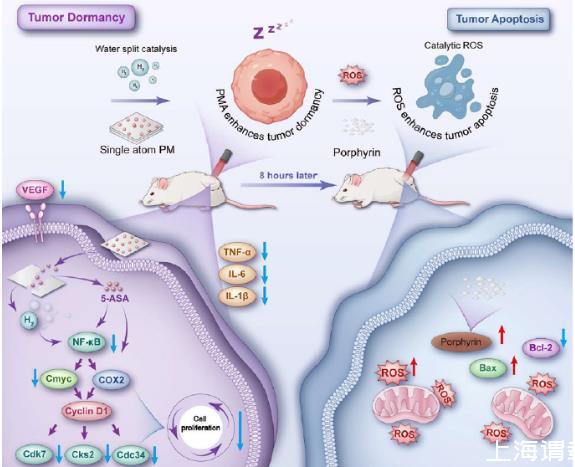
圖1、抑制NF-κB信號調控相關通路,重編程腫瘤免疫微環境,從而誘導腫瘤生長抑制,建立“類休眠”狀態。
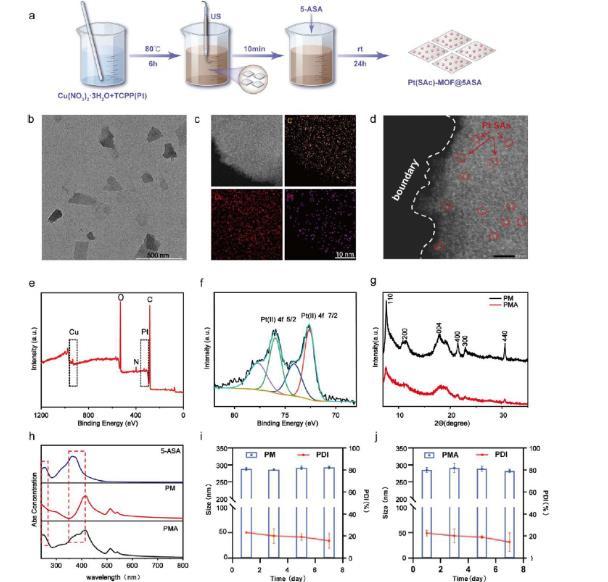
圖2、PMA非必需品的合成與表征。(a)Pt-SAs-MOF 5-ASA合成方案。(b)Pt-SA-MOF 5-ASA非分子的TEM圖像。(c)通過超聲處理實現PMA的EDS定位。(d)對PMA中Pt單原子進行明場高分辨率透射電子顯微鏡。(e,f)PMA的XPS光譜和Pt(4f)的高分辨率XPS光譜。(g)PM和PMA的XRD模式。(h)PM在5-ASA加載前后UV–vis吸收光譜。(i,j)PM和PMA的動態光散射(DLS)(n=3)。
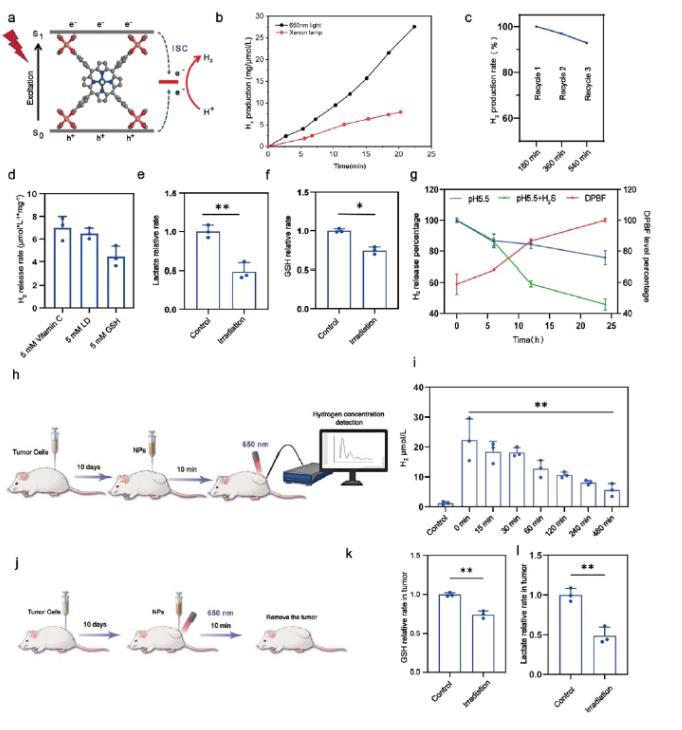
圖3、體外和體內氫氣生成的檢測。(a)催化氫氣生產過程示意圖。(b)材料對氫氣生產的性能測試。(c)材料循環性能。(d)使用不同基底犧牲劑的氫氣生產速率(n=3)。(e,f)乳酸和GSH作為底物在體外氫產生前后濃度變化(n=3)。(g)模擬體內環境下H2生成性能的變化及卟啉釋放后ROS生成。(h,i)體內H2濃度的原位測量(n=3)。(j)H2生成的實時體內監測。小鼠腫瘤內光催化犧牲劑含量檢測流程圖。(k,l)腫瘤攜帶小鼠治療前后乳酸和GSH作為底物的體內濃度變化(n=3)。
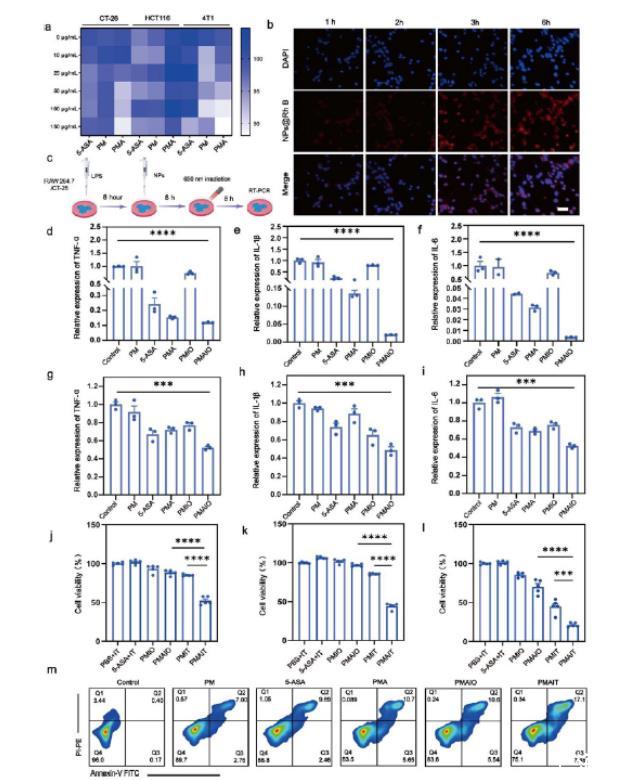
圖4、PMA光催化氫的腫瘤微環境調控。(a)三種不同細胞系(CT-26、HCT116和4T1)中PM、PMA和5-ASA的細胞毒性評估(b)裝載羅達敏B標記PMA(50微米尺)細胞的吞噬分析。(n=5)。(c)巨噬細胞Raw246.7和CT-26細胞氫氣生產測定流程圖。(D–F)巨噬細胞Raw246.7在納米材料培養后炎癥因子的變化(n=3)。(G–i)用納米材料培養后CT-26細胞炎癥因子的變化以產生氫氣。(J–L)評估雙重照射策略在CT-26、HCT116和4T1細胞(n=5)中的細胞層面治療療效。(m)通過流式細胞術測量了細胞存活率和雙重照射策略的存活率。(n=3)。其中包括:IO:照射一次,IT:照射兩次,PMIO:PMA+照射一次,PMAIO:PM+照射一次,PMIT:PM+照射兩次,PMAIT:PM+照射兩次。數據以標準差±均值表示。
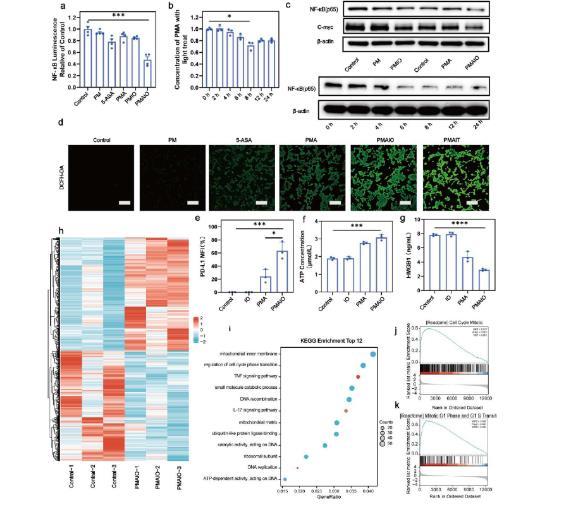
圖5、通過PMA對NF-κB信號通路進行時空調控。(a)細胞轉染后用NF-kB熒光素酶報告質粒檢測化學發光(n=3)。(b)在不同時間點(n=3)檢測到NF-κB表達。(c)單次照射H2生成及藥物負載光調制后NF-κB蛋白動力學的Western blot分析。(d)驗證在雙重照射策略和休眠誘導后重新照明細胞時的ROS產生,比例尺條:100微米。(e)PD-L1表達水平的流式細胞術分析,并得出相應的統計結果(n=3)。(f)ATP濃度變化(n=3)。(g)ELISA檢測HMGB1蛋白水平變化(n=3)。(h)來自指示組mRNA測序處理樣本的熱圖(n=3)。(i)京都基因與基因組百科全書(KEGG)通過途徑分類,用于揭示上述差異表達基因受影響的途徑(前12名)。(j,k)細胞周期有絲分裂和有絲分裂G1期及G1S轉變的富集結果(n=3)。其中包括IO:一次照射,PMIO:PM+照射一次,以及PMAIO:PMA+照射一次。
結論與展望
本論文成功開發并驗證了一種名為PMA的納米生物催化劑,它通過誘導腫瘤休眠與催化活性氧(ROS)風暴的協同作用,為結直腸癌治療提供了一種創新且有效的雙模態治療策略。研究證實基于鉑單原子催化劑(SACs)的PMA納米平臺能夠在可見光(650 nm激光)照射下,利用腫瘤微環境(TME)中的內源性物質(如乳酸、谷胱甘肽)作為犧牲劑,實現時空可控的氫氣(H?)生成。所產生的H?通過抑制關鍵的NF-κB信號通路,有效地將活躍的腫瘤細胞轉變為增殖停滯、代謝靜息的“休眠樣”狀態。這種休眠狀態并非終點,而是使腫瘤細胞對氧化應激的敏感性顯著增加,為后續的精準打擊創造了條件。本研究不僅提出了“先誘導休眠,后精準清除”的腫瘤治療新范式,還展示了單原子催化劑在生物醫學領域,特別是氣體治療中的巨大應用價值。它將納米催化劑的精準催化功能與免疫調節相結合,為干預腫瘤進展提供了一個通過協調細胞周期控制和微環境重編程的創新框架。盡管該策略對淺表腫瘤效果顯著,但對于深部腫瘤,未來或可探索通過光纖導入或X射線激活等minimally invasive方式來實現體內催化反應。Unisense微電極作為一種高精度、實時的氣體濃度檢測工具,對驗證PMA納米平臺在體內外的時空可控產氫能力起到了至關重要的作用。Unisense微電極提供的直接、實時的氫濃度數據,是證明PMA納米平臺能否按設計在復雜生物環境中工作的最有力證據。它證實了“雙次光照”策略的合理性——首次光照可引發顯著的H?生成。Unisense微電極監測到的H?動力學曲線與材料降解、藥物釋放的時間點高度吻合,幫助研究者清晰地勾勒出完整的治療鏈條:產氫誘導休眠→材料降解釋放光敏劑→再次光照產生ROS清除休眠細胞。本研究工作為結直腸癌的精準催化治療開辟了新的道路。
 相關新聞
相關新聞