熱線:021-66110810,66110819
手機(jī):13564362870


熱線:021-66110810,66110819
手機(jī):13564362870
材料與方法
標(biāo)本
采集常見尺寸(體長(zhǎng)約30毫米)的標(biāo)本,來自美國(guó)路易斯安那州巴吞魯日(30°24.98'N 91°7.18'W)的一根橡木原木,并將其與采集時(shí)所在的木塊一起保存在單獨(dú)的容器中。解剖和細(xì)菌/古菌群落鑒定在采集日期后約2周進(jìn)行。
甲蟲解剖、DNA提取和pH測(cè)量
將甲蟲在95%乙醇中浸泡2分鐘進(jìn)行表面消毒,然后用無菌磷酸鹽緩沖鹽水清洗。在無菌磷酸鹽緩沖鹽水中解剖單個(gè)甲蟲,首先去除鞘翅以暴露膜質(zhì)背側(cè)。隨后,去除翅膀,解剖角質(zhì)膜以暴露腹腔內(nèi)的自然腸道排列(圖1)。然后取出整個(gè)腸道,拉伸并切成四個(gè)區(qū)域(前腸-FG、中腸-MG、前中腸-AHG、后后腸-PHG;圖1b)。將每個(gè)區(qū)域放入1ml RNALater(Qiagen,Valencia,CA,USA)中,并在提取前于4°C儲(chǔ)存過夜。通過將每個(gè)腸道區(qū)域在含有750μl RLT(硫氰酸胍)緩沖液(Qiagen)的Lysing Matrix E管(Qbiogene Inc.,Carlsbad,CA,USA)中珠磨30秒(5.5 m s-1),冷卻1分鐘,再重復(fù)該過程30秒,制備粗提物。使用標(biāo)準(zhǔn)酚-氯仿相分離技術(shù)從混合物中分離核酸,并用乙醇沉淀。使用AllPrep DNA/RNA Kit(Qiagen)根據(jù)制造商說明進(jìn)一步純化粗核酸提取物,以同時(shí)分離DNA和RNA組分。在另一組四只甲蟲中,通過解剖出每個(gè)部分并將腸道內(nèi)容物在30%水(w v-1)中勻漿,再用微電極測(cè)量每個(gè)腸道區(qū)域的pH。

用于PhyloChip分析的PCR擴(kuò)增
我們的實(shí)驗(yàn)包括四只甲蟲(重復(fù))和每只甲蟲的四個(gè)腸道區(qū)域(16個(gè)樣本)。每個(gè)樣本進(jìn)行三次重復(fù)反應(yīng),使用三種不同的退火溫度進(jìn)行聚合酶鏈?zhǔn)椒磻?yīng)(PCR)擴(kuò)增,使用5μl 1 x Takara ExTaq PCR緩沖液(含MgCl2)、300 pM引物27F(5'-GTTTGATCCTGGCTCAG-3')和1492R(5'-GGTTACCTTGTTACGACTT-3')用于細(xì)菌,1492R和4F(5'-TCCGGTTGATCCTGCCRG-3')用于古菌,50μg牛血清白蛋白,200μM dNTPs,2.5 U ExTaq DNA聚合酶(Takara Mirus Bio Inc.,Madison,WI,USA),5ng模板和milliQ H2O補(bǔ)足至50μl體積。PCR循環(huán)條件為:95°C初始變性3分鐘,然后進(jìn)行25個(gè)循環(huán):95°C 30秒,退火48°C、53°C和56°C 25秒,72°C延伸2分鐘,最后72°C延伸10分鐘。將三種不同退火溫度的產(chǎn)物(150μl)合并,并使用乙醇沉淀(15μl 3M乙酸鈉和300μl 100%乙醇)進(jìn)行濃縮。將沉淀重懸于TE(Tris-EDTA)緩沖液中,并在通過凝膠電泳定量前使用PCR純化試劑盒(Qiagen)進(jìn)行純化。
PhyloChip雜交和樣本檢測(cè)
微陣列構(gòu)建、標(biāo)記、雜交、檢測(cè)和定量方法由Brodie等人詳細(xì)描述。G2 PhyloChip包含超過300,000個(gè)探針,靶向8741個(gè)細(xì)菌和古菌分類群。從合并的PCR反應(yīng)中,取200ng細(xì)菌和50ng古菌PCR產(chǎn)物,用DNAse I片段化,生物素標(biāo)記,根據(jù)制造商推薦的方案進(jìn)行雜交、洗滌和染色。總共分析了16個(gè)微陣列。每個(gè)PhyloChip被掃描并記錄為像素圖像,使用標(biāo)準(zhǔn)Affymetrix軟件(GeneChip微陣列分析套件,版本5.1,Santa Clara,CA,USA)進(jìn)行初始數(shù)據(jù)采集和強(qiáng)度測(cè)定。當(dāng)某個(gè)分類群/OTU(操作分類單元)超過90%的指定探針對(duì)在至少三個(gè)重復(fù)(每個(gè)腸道區(qū)域四個(gè)重復(fù))中呈陽性時(shí),則認(rèn)為該分類群存在于樣本中。
PhyloChip檢測(cè)的統(tǒng)計(jì)分析
所有統(tǒng)計(jì)分析均在R編程環(huán)境(The R Development Core Team,2010)中進(jìn)行。對(duì)與擴(kuò)增子靶標(biāo)定量相關(guān)的變異以及下游與靶標(biāo)片段化、標(biāo)記、雜交、洗滌、染色和掃描相關(guān)的變異進(jìn)行了校正,具體方法詳見Ivanov等人。使用方差分析檢驗(yàn)每個(gè)分類群/OTU在四個(gè)腸道區(qū)域中的強(qiáng)度是否顯著。使用Benjamini-Hochberg錯(cuò)誤發(fā)現(xiàn)率程序?qū)Φ玫降腜值進(jìn)行多重檢驗(yàn)校正。使用Goldfarb等人中詳述的方法生成檢測(cè)到的細(xì)菌分類群的系統(tǒng)發(fā)育樹,并使用交互式生命樹網(wǎng)絡(luò)服務(wù)器進(jìn)行可視化和注釋。
系統(tǒng)發(fā)育群落分析
使用Picante R包進(jìn)行系統(tǒng)發(fā)育群落分析。使用G2 PhyloChip靶向序列的最大似然RAxML樹作為初始樹。從未在腸道區(qū)域檢測(cè)到或具有模糊名稱的分類群從樹中修剪掉,得到一個(gè)包含1382個(gè)分類群的樹。我們使用了末端洗牌零模型(模型1),運(yùn)行10000次重復(fù)。在該模型中,末端(單個(gè)分類群)在整個(gè)系統(tǒng)發(fā)育中洗牌,并將得到的指標(biāo)與觀察值進(jìn)行比較,α=0.05。末端洗牌模型被確定對(duì)Phylocom分析具有穩(wěn)健性,且I類錯(cuò)誤(假陽性)水平較低。我們使用凈親緣關(guān)系指數(shù)(NRI)指標(biāo)來比較不同腸道區(qū)域微生物群落的系統(tǒng)發(fā)育聚類。我們還確定了系統(tǒng)發(fā)育多樣性(PD)和香農(nóng)多樣性指數(shù)(H';表1)。
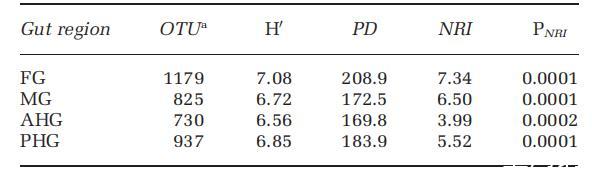
表1 鍬甲蟲腸道各區(qū)域的系統(tǒng)發(fā)育群落指標(biāo)0. disjunctus腸道菌群的多樣性與功能
通過15N2摻入確認(rèn)固氮作用
將四只甲蟲放入一個(gè)麻醉箱中,該箱連接到一個(gè)裝有66 ml O2的氣球,并用99原子%15N2沖洗以達(dá)到約78%的N2濃度。孵育12天后,對(duì)箱子進(jìn)行吹掃,取出甲蟲進(jìn)行解剖和核酸提取,方法同上。通過將提取物移液到錫膠囊中的Chromosorb W(Advanced Minerals,Santa Clara,CA,USA)上,制備用于同位素分析的RNA提取物。使用RoboPrep-CN分析儀與20-20型同位素比質(zhì)譜儀(Sercon Ltd.,Cheshire,UK)聯(lián)用,分析樣品的N含量和δ15N。
 相關(guān)新聞
相關(guān)新聞