熱線:021-66110810,66110819
手機:13564362870


熱線:021-66110810,66110819
手機:13564362870
GO與HA的相互作用。如圖S17(支持信息)所示,與GO譜圖相比,GO-HA的C=C基團出現約40 cm?1的藍移(從1608 cm?1移至1645 cm?1),且1396 cm?1處的羥基峰強度減弱。傅里葉變換紅外光譜表明HA可能通過π-π相互作用定位于GO的sp2平面,這與Hu等人關于石墨烯的研究以及Yang等人關于少層還原氧化石墨烯的結論一致。為進一步分析GO與HA的相互作用,進行了透射電鏡(TEM)、掃描電鏡(SEM)和原子力顯微鏡(AFM)測試。圖4a、b及支持信息中的圖S1、S18顯示,GO片層光滑透明,而GO-HA在納米片上呈現黑色斑點與顆粒。在透射電鏡(TEM)和掃描電鏡(SEM)圖像中分別可見。此外,氧化石墨烯(GO)片層邊緣變得平滑,厚度范圍收窄至2.0-8.9納米。這些數據證實了腐植酸(HA)在GO片層表面的固定作用。圖4c所示的拉曼光譜(RS)中,G峰和D峰分別對應GO的sp2(1358 cm?1)和sp3(1695 cm?1)碳體系。GO與GO-HA的D/G峰強度比分別為0.88±0.03和0.76±0.02,表明HA的吸附顯著降低了GO的無序結構(p<0.05)。通過動態光散射測定Zeta電位(分散性)顯示(圖4d),GO和GO-HA的Zeta電位隨pH值升高而降低,說明兩種材料在E3溶液中pH 2.0-12.0范圍內表面均帶負電荷。Zeta電位結果還表明GO-HA比GO帶有更多負電荷且分散性更佳。粒徑分布結果(圖4e)顯示GO和GO-HA的粒徑分布范圍分別為192.8-531.25 nm(平均尺寸323.2±23.7 nm)和220.2-481.4 nm(平均尺寸356.1±29.1 nm)。24小時后,GO和GO-HA的平均尺寸分別增至825.8 nm和394.4 nm。上述結果證實HA通過增加表面負電荷增強了GO的分散性。
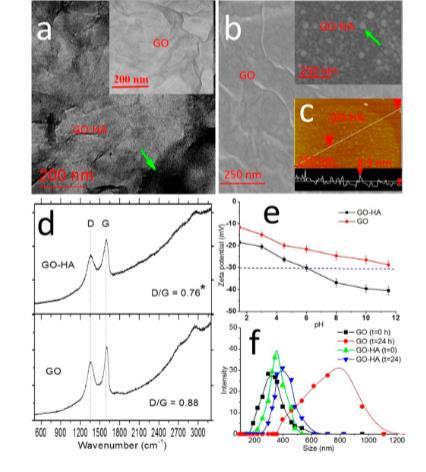
圖4. GO與HA的相互作用。(a) GO-HA的透射電鏡圖像;(b) GO和GO-HA的掃描電鏡圖像;(c) GO-HA的原子力顯微鏡圖像;(d) GO和GO-HA的拉曼光譜;(e) Zeta電位隨pH的變化;(f) GO和GO-HA在0和24小時的尺寸分布變化。綠色箭頭指示HA。
討論
為了探索HA對GO納米毒性的影響,研究了GO/GO-HA與卵膜界面的相互作用、卵膜蛋白的改變、納米材料的吸收和沉積以及線粒體毒性和氧化應激。測試的HA濃度(0.01-100 mg/L)具有環境相關性。本研究指出HA大大降低了GO的潛在風險。斑馬魚卵膜由糖基化蛋白質組成,保護胚胎并作為抵御納米顆粒的第一道屏障。在本研究中,觀察到GO緊密粘附在卵膜表面,相互作用界面高達86.7%,這阻塞了卵膜孔并導致卵膜間隙內出現缺氧微環境。缺氧在斑馬魚胚胎發生過程中誘導缺血、孵化延遲和畸形。ROS不是納米毒性的唯一因素,并且在細菌和精子中也發現了GO對生物體表面的包裹。因此,將胚胎困在聚集的GO片中以使其與環境隔離被認為是GO對生物體毒性的可能機制。然而,在HA存在下,GO與卵膜的相互作用界面變得松散并顯著減少,卵膜間隙內的氧濃度恢復正常水平。相應地,在GO-HA孵育的胚胎中,孵化率增加,心包水腫發生率降低。
此外,在GO處理的胚胎中,卵膜的蛋白質二級結構被顯著改變。在這些胚胎中觀察到的β-折疊結構增加和α-螺旋結構減少與鉛、氰化物和輻射暴露的不利效應相似。早期工作表明,蛋白質中所有組成氨基酸側鏈都易受自由基影響,并且它們的二級結構可能因自由基攻擊而改變。在本研究中,產生的·OH可能攻擊了蛋白質的側鏈氨基酸,導致蛋白質二級結構改變。此外,GO的g值為2.0031,與自由電子(2.0023)相似,表明GO由于碳缺陷(如懸空鍵以及邊緣或內部平面上的轉折和扭結)具有觸發ROS形成的潛力。相反,在HA存在下,·OH的產生和GO-HA與卵膜的相互作用界面顯著減少。相應地,暴露于GO-HA的胚胎中卵膜蛋白質二級結構恢復。此外,卵膜突起被GO破壞并在HA存在下恢復。綜上所述,這些結果表明HA顯著減輕了GO誘導的卵膜損傷。
卵膜中的自然孔徑約為0.5至1μm,這足夠大以允許許多納米顆粒進入卵膜囊。鑒于TEM圖像中的尖銳邊緣和GO優異的機械性能,GO容易通過孔隙穿透生物膜進入卵膜,這已被廣泛提出。HA固定化后,GO的厚度增加,鋸齒狀邊緣消失并增強折疊;膜穿透被減輕,導致GO-HA的吸收主要通過卵膜孔進行。此外,GO誘導的卵膜損傷,如蛋白質二級結構的改變和突起的塌陷,促進了納米材料在卵膜囊中的吸收。相比之下,在HA存在下,進入卵膜囊的GO較少,如TEM、RS和共聚焦顯微鏡所示。這些數據暗示卵膜可能具有控制GO和GO-HA吸收的潛力。為了檢查GO-HA吸附到塑料孔板上的可能性,研究了GO-HA在塑料孔板上的吸附。支持GO-HA在塑料孔板上沒有明顯吸附,表明GO-HA在塑料孔板上的吸附不能解釋胚胎對GO吸收的減少,并且卵膜控制了GO的吸收。最近的一份報告發現,除了作為物理屏障外,卵膜還是一種化學反應性膜,可控制銀的原位形態,支持我們的提議。此外,卵膜可能通過整體蛋白質模式的變化來響應外部刺激,這可能涉及一個生化過程,盡管潛在機制尚不清楚。然而,這些數據表明HA可以調節GO的形態和吸收,增強卵膜的保護作用,并降低GO在斑馬魚胚胎發生過程中的毒性。
納米材料進入胚胎后,GO和GO-HA表現出不同的沉積模式。GO的聚集在胚胎的卵黃細胞和深層細胞中很明顯。相比之下,GO-HA沉積物更小更少,并且主要位于上皮包被層細胞中,這些細胞起保護作用并抑制周皮的獨有生成。與上皮包被層細胞相比,卵黃細胞和深層細胞在胚胎發生中起重要作用。前者在早期階段提供營養并介導細胞增殖和分化,后者是胚胎發生的主要區域。這些數據表明HA的存在導致GO易位到相對不重要的組織,這與HA介導的增強石墨烯在小麥液泡中的儲存一致。易位機制可能涉及納米材料的形狀和親水性,因為GO表現出更好的親脂特性和尖銳的鋸齒狀邊緣,因此可能比GO-HA更容易穿透細胞膜并在細胞質中聚集。
GO包裹引起的缺氧和具有鋸齒狀邊緣的物理損傷都可能導致線粒體損傷。事實上,100 mg/L GO確實誘導了顯著的線粒體損傷,而HA顯著減輕了上述不利影響。此外,建議保持石墨烯基材料的穩定分散以最小化其毒性。Zeta電位表明GO-HA在生理相關pH范圍6-10內比GO表現出更多的負電荷并且更穩定。因此,GO-HA也可能通過增加表面負電荷并減少其通過電荷排斥與胚胎、線粒體和其他細胞結構的接觸來降低GO在斑馬魚胚胎發生過程中的毒性。
線粒體損傷與自由基生成及氧化應激增強密切相關,這已被提出作為納米毒性的主要機制。在氧化石墨烯暴露組中,胚胎內活性氧(ROS)生成量較對照組和GO-HA組顯著增加(p<0.05),這可能破壞由酶性和非酶性防御系統維持的自由基動態平衡。一致地,與對照組和GO-HA組相比,GO顯著誘導SOD水平升高和GSH水平降低(p<0.05)。此外,傅里葉變換紅外光譜(FT-IR)結果表明,經GO處理的胚胎中DNA和蛋白質均受損,這與蛋白質羰基化和8-羥基脫氧鳥苷(8-OHdG)加合物的數據一致。近期研究顯示GO會引發斑馬魚DNA中8-OHdG修飾,與我們的結果相符。然而在腐植酸(HA)存在的情況下,GO引發的上述負面效應得到緩解,且測試的抗氧化酶活性得以恢復。這些數據表明HA通過修復線粒體損傷來降低GO誘導的氧化應激。
環境影響
本研究發現,腐植酸(HA)改變了氧化石墨烯(GO)的表面形態,并提高了其在生理和環境相關pH值范圍6-10下的穩定性。HA通過減弱GO與卵殼膜的相互作用,恢復了胚胎卵殼微環境中的氧含量。此外,HA影響了GO的攝取和轉運,表明其對硬骨魚胚胎發生具有解毒作用。HA減輕了GO誘導的胚胎線粒體損傷、形態學改變及氧化應激。上述結果表明HA改變了GO的命運和生物響應。鑒于HA在天然水體中的廣泛分布,其可作為GO的天然解毒劑。本研究也提示,此前未考慮HA暴露的納米材料生態風險評估研究需要重新審視。
 相關新聞
相關新聞